Ацетонемічний синдром дітей тактичні кроки доктора-практика
В.В. Бережной, В.В. Корнева, В.Г. Козачук, Л.В. Курило, Е.А. Боярская, М.А. Капичина, А.В. Чоботарь
Национальная медицинская академия последипломного образования им. П.Л. Шупика, г. Киев Киевская городская детская клиническая больница №1
Resume. В статье предложены критерии подхода к ранней диагностике ацетонемического синдрома у детей, которые позволят семейным врачам и педиатрам своевременно диагностировать первичный ацетонемический синдром (синдром циклической рвоты — CVS): детализация семейного анамнеза; детализация анамнеза болезни и жизни у ребенка; аде- кватная оценка ведущих симптомов во внеприступном периоде. Знание этих клинико-анамнестических показателей позволит своевременно и адекватно начать стартовую терапию ацетонемическогосиндрома у детей (как первичного, так и вторичного характера) с высокоэффективного регидратационного средства — Регидрон Оптим вкомбинации с энтеросорбентом 4 поколения — препаратом Атоксил.
Keywords: ацетонемический синдром, дети, регидратационная терапия, Регидрон Оптим, энтеросорбция, Атоксил.
Introduction
Ацетонемический синдром детей (АСД) — одно из самых распространенных заболеваний детского возраста,которое проявляется стереотипными повторны- ми эпизодами рвоты, чередующимися с периодами полного благополучия.
Большинство отечественных педиатров выделяют две разновидности АСД — первичный и вторичный [1,4,6,7].
Первичный АСД встречается у детей с нейро-артритической аномалией конституции (мочекислым диатезом) и характеризуется нарушением пуринового обмена с избыточной продукцией мочевой кислоты и ее предшественников, неустойчивостью углеводного и липидного обмена (со склонностью к кетозу), лабильностью медиаторных функций нервной системы, определяющих особенности ее реакций. Возникает АСД преимущественно у детей в возрасте от 2 до 10 лет и проявляется гиперурикемией и периодическими метаболическими (ацетонемическими) кризами с развитием гиперкетонемии, ацетонурии, ацидо- за. Но в последние годы все чаще такие состояния продолжаются и в подростковом возрасте.
Вторичный АСД наиболее часто возникает при: инфекционном токсикозе; сочетанной патологии желудочно-кишечного тракта, сопровождающейся симптомами интоксикации, холестаза; токсическом поражении печени; при нарушении микрофлоры кишечника. Причиной вторичного АСД может быть также: голодание, декомпенсированный сахарный диабет, гиперинсулинизм, инсулиновая гипогликемия, гликогеновая болезнь, тиреотоксикоз, черепно-мозговая травма, опухоль мозга в области турецкого седла, болезнь Иценко—Кушинга, лейкемия, гемолитическая анемия и другие состояниях. Клническая картина ацетонемического синдрома в таких случаях определяется основным заболеванием, на которое наслаивается кетонемия [6].
Литературные данные о распространенности первичного и вторичного АСД разноречивы. Так, А.С. Сенаторова, Е.В. Осипенко (2007) [12] считают, что вторичный АСД встречается у детей в 2 раза чаще, чем первичный. Аналогичные данные приводят Л.В. Квашнина Н.Б. Евграфова (2003) [6]. I. Booth, R. Cunha Ferreira, J. F. Desjeux et al. (1992) [16] в своих исследованиях показали, что первичный АСД в педиатрии встречается в 2,4 раза чаще, чем вторичный ситуационный ацетонемический синдром.
Особенностями АСД является высокая лабильность метаболических и водно-электролитных изменений, взаимосвязь с фоновыми состояниями и вегетативными синдромами, присущими детям разных возрастных групп.
Метаболической основой развития кетоацидоза является усиленный липолиз, приводящий к поступлению в печень большого количества жирных кислот. Ограниченные возможности утилизации продуктов липолиза приводят к избыточному образованию кетоновых тел — ацетона, ацетоуксусной и бета-оксимасляной кислот, которые раздражают слизистую оболочку пищевого канала, что обуславливает боль в животе и рвоту.
Кетоновые тела также вызывают развитие метаболического ацидоза, что приводит к: нарушению гемодинамики (периферический вазоспазм) и вытекающая из этого относительная гиповолемия, которая в дальнейшем усиливается рвотой; наркоподобному влиянию на центральную нервную систему. Кетоновые тела провоцируют компенсаторную гипервентиляцию (гиперкапнию), появляется запах ацетона при дыхании, обнаруживаются кетоновые тела в моче. В результате формируется типичная картина ацетонемического синдрома [11].
Развитие и течение АСД усугубляют: нервно-артритический диатез; заболевания печени (нарушение липолиза); патология канальцевой системы почек (нарушение КОС); болезни поджелудочной железы (функциональный дефицит инсулина, нарушения экзокринной функции); изменения в легких (участие в компенсаторной одышке). Возникающая при этих состояниях рвота, перспиративные потери жидкости за счет одышки влекут выраженные нарушения электролитного баланса у детей [5,6].
Следует отметить, что в последнее десятилетие большинство исследователей первичного АСД трактуют это состояние как «синдром циклической рвоты» (CVS). Большинство педиатров и семейных врачей осознают общность в большинстве механизмов этиологии и патогенеза, ведущих клинических симптомов данных состояний. Введение протокола «Синдром циклической рвоты» (приказ МЗ Украины №438 от 26.05.2010 г. «Протоколы диагностики и лечения заболеваний органов пищеварения у детей») нацелит педиатров, семейных врачей на анализсемейного анамнеза, в частности в вопросах взаимосвязи с мигренью и другими патогенетически близкими состояниями [11,13]. Однако ряд протокольных подходов в лечении АСД, особенно наамбулаторно-поликлиническом этапе, на протяжении 2010–2011 гг. подвергались критике медицинской общественностью. Новый вариант Протоколов позволит максимально приблизить современные этиопатогенетические подходы в лечении АСД и реальными возможностями леченияэтого состояния в Украине.
Многолетний опыт педиатрической службы по купированию АСД, особенно на амбулаторно-поликлиническом этапе, свидетельствует о высокой эффективности оральной регидратации у большинства пациентов при АСД [1,12,15].
Выраженность метаболических и водно-электролитных изменений, лабильность этих процессов мотивирует педиатров к поиску оптимальных методов лечения АСД, доступных как для амбулаторно-поликлинической, так и для госпитальной практики.
К таким методам относиться применение в комплексном лечении АСД оральной регидратационной терапии в сочетании с современными энтеросорбентами. Такая тактика позволит быстро купировать основные симптомы АСД — метаболические и водно-электролитные изменения.
Многие годы бесспорным лидером при проведении оральной регидратационной терапии был и есть препарат «Регидрон» (Rehydron), а с 2010 г. в Украине широко используется и его педиатрическая форма — Регидрон Оптим.
Как показали работы ряда авторов, несмотря на непродолжительность нахождения на фармацевтическом рынке Украины, Регидрон Оптим достаточно широко применяется в качестве регидратационного средства в практике педиатров и семейных врачей [1].
Регидрон Оптим (REHYDRON OPTIM) Orion — препарат, в состав которого на 1 л раствора входят: натрия хлорид — 2,60 г (44,444 ммоль/л),натрия цитрат — 2,90 г (29,565 ммоль/л), калия хлорид — 1,5 г (20,134 ммоль/л), глюкоза безводная — 13,5 г (74.92 ммоль/л). Вспомогательные вещества: калия ацесульфам, ароматизатор лимонный. Осмолярность раствора Регидрона Оптим — 245 мосм/л. Состав раствора Регидрон Оптимполностью соответствует международным стандартам, в частности рекомендациям Европейского Общества детской гастроэнтерологии и питания (ESPGAN).
Удобна и форма выпуска — 1 пакетик на 500 мл готового раствора. В упаковке 6 пакетиков, из которых можно приготовить 3 л регидратационного раствора. Это количество раствора в большинств еслучаев является оптимальной курсовой дозой для детей раннего возраста. Следует отметить, что ароматизатор лимонный является безаллергенным компонентом раствора. Оптимален и возраст начала приема этого препарата — с рождения. При тошноте и рвоте Регидрон Оптим целесообразно принимать в охлажденном виде в небольших повторяющихся дозах. Рекомендованная суточная доза на 10 кг веса — не менее 0,5 л раствора Регидрон Оптим, что равно 1 пакетику (информация взята из Компендиума it-apharm.ru 2009–2010). При необходимости эта доза повышается в полтора-два раза.
Следует отметить, что регидратационная терапия при АСД, согласно рекомендации многих исследователей, назначается индивидуально в зависимости от возраста, массы тела и степени обезвоживани яорганизма. В первые 6 часов лечения объем оральных растворов солей (ОРС) составляет 20–30 мл/кг массы тела. Общий объем жидкости за первые 6 часов регидратационной терапии составляет в большинстве случаев 30–40 мл/кг, а в случае необходимости — до 60 мл/кг [11,12].
Суточный объем жидкости в первые 1–3 дня лечения составляет от 60 мл/кг до 100 мл/кг массы тела ребенка. Из этого количества ОРС должен быть не менее 70%. Помимо этого возможно употребление и других жидкостей (отвары сухофруктов, кипяченая вода, дегазированная щелочная минеральная вода) [4,7]. Растворы при необходимости следует принимать в небольшом количестве (чайная или столовая ложка в зависимости от возраста) каждые 5–15 минут, затем можно постепенно повышать разовую дозу.
Кроме оральной регидратационной терапии, которую целесообразно начинать еще до развития рвоты, в частности при развитии у ребенка вялости, снижения аппетита, очень важно в этот же период подключить энтеросорбенты [7,14].
Основная цель назначения энтеросорбентов, как в продромальном периоде АСД, так и в периоде приступа, — это проведение детоксикации, улучшение эвакуационной функции желудка.
К таким энтеросорбентам относится Атоксил — препарат нового, 4-го, поколения сорбентов (Кремния диоксид «Орисил®», производства ТОВ «Орисил», который прошел тест на соответствие стандартам FDA и фармакопеи USA по монографным тестам USP29 — NF24) [2,3,8].
Главной особенностью препарата Атоксил (кремневого сверхвысокодисперстного непористого сорбента) является его белковосорбционная способность, благодаря которой происходит связывание, инактивация и выведение из организма экзо- и эндотоксинов, аллергенов, антигенов, продуктов деградации некротических тканей и других вредных веществ белкового происхождения. Эти особенности препарата Атоксил обеспечивают мощный детоксикационный эффект.
В сравнении с другими сорбентами (угольными, органическими полимерами) Атоксил обладает наивысшей площадью активной поверхности сорбции, около 400 м2/г. Благодаря этим свойствам Атоксил обеспечивает быстрое снижение эндогенной интоксикации уже с первого приема препарата. За счет непористости пик активности препарата отмечается уже через 4 минуты после его приема [2,9,10].
В случаях вторичного АСД, возникшего на фоне вирусной диареи или ОКИ, терапевтический эффект препарата Атоксил обусловлен также его способностью связывать микроорганизмы и вирусы с активностью до 1010 микробных тел на 1 г. Благодаря этому происходит адсорбциямикробов и вирусов, бактериостатическое и, опосредовано, бактерицидное действие, торможение инвазии патогенной микрофлоры через слизистую желудочно-кишечного тракта, что предупреждает развитие эндотоксикоза, быстро устраняет основную симптоматику заболевания [3,9,10].
Препарат Атоксил имеет высокий профиль безопасности, поэтому рекомендован детям с 1 года жизни. В отличие от угольных сорбентов, не травмирует слизистую желудка, полностью выводится из организма. Ему присуща также гипоаллергенность. По сравнению с существующими сорбентами Атоксил обладает значительно лучшими органолептическими свойствами. Препарат легко принимается детьми и взрослыми [3,8].
Рекомендуемые дозы Атоксила у детей: 1–2 года — разовая доза — 1 г препарата, средняя суточная доза — 2 г; 2–4 года разовая доза — 1 г,средняя суточная доза — 3 г; 4–7 лет — разовая доза — 2 г, средняя суточная доза — 4 г;
Table 1
Возрастной состав обследованных больных
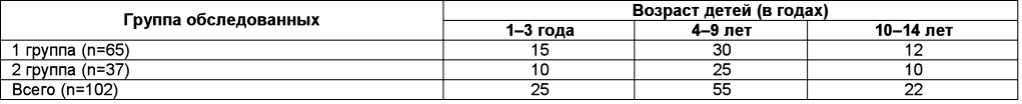
Fig.1. Варианты ацетонемического синдрома у обследуемых детей 7–12 лет — разовая доза — 2 г, средняя суточная доза — 5–6 г; дети старше 12 лет — разовая доза — 4 г, средняя суточная доза — до 8 г.
Все вышеприведенное мотивировало нас к внедрению и изучению эффективности препаратов Регидрон Оптим и Атоксил при лечении АСД. Работа проведена на базе Киевской городской детской клинической больницы № 1 (главный врач — Ю.А. Кожара), которая является клнической базой кафедры педиатрии №2 НМАПО им. П.Л. Шупика (заведующий кафедры — профессор В.В. Бережной). Исследованиепроводилось в 2011–2012 гг.
Materials and research methods
В отделении гастроэнтерологии, а также у пациентов консультативной поликлиники препараты Атоксил и Регидрон Оптим использовались в комплексной терапии 65 детей с ацетонемическим синдромом (группа 1). У 37 пациентов при АСД в терапии использовалось щелочное питье или другие оральные растворы, энтеросорбент Атоксил не назначался (группа 2). Диагностика ацетонемии проводилась с помощью полосок CITOLAB К (кето- ны) от компании «Фармаско».
Возраст пациентов во всех группах был от 1 года до 14 лет (табл. 1). Деление по полу и возрасту в обеих группах было относительно эквивалентным.
Вторичный АСД был зарегистрирован у 60 детей 1 и 2 групп с нечастыми (отсутствие цикличности) или одноразовими эпизодами ацетонемической рвоты. Этот синдром возникал на фоне: ОРВИ с гипертермическим синдромом, при дебюте вирусной диареи; функциональной диспепсии, ДЖВП, при проведении дегельминтизации, при пищевых аллергических реакциях. В таких случаях АСД определялся основным заболеванием, на которое наслаивалась кетонемия.
В группу первичного АСД вошли 42 пациентов с проявлениями мочесолевого (мочекислого) диатеза. У этих детей в 80% случаях были изменения при исследовании транспорта солей, подтверждающие поставленный диагноз.
Research results and their discussion
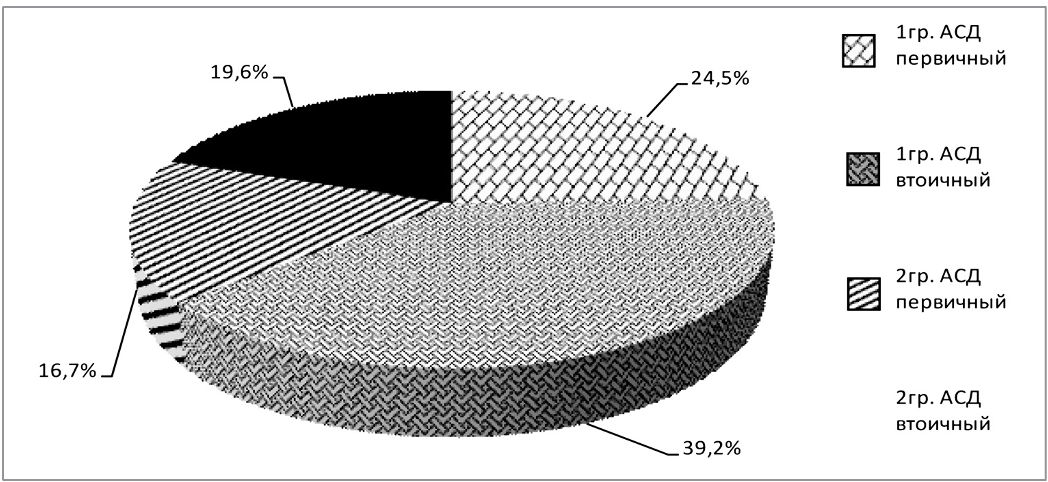
У детей при первичном ацетонемическом синдроме отмечалась цикличность рвоты с удовлетворительными межприступными периодами. У 34 пациентов 1 и 2 групп с первичным АСД (80%) преобладали приступообразные мигренеподобные головные боли, причем возраст у этих пациентов был старше 9 лет. У этих же детей были эпизоды пароксизмальной вегетативной недостаточности. Подробный анамнестический спектр жалоб и особенности симптомов внеприступного периода у пациентов при первичном АСД (CVS) представлены на рисунке 2.
Учитывая вышеприведенные данные, у всех обследованных, вошедших в группу первичного АСД, согласно Римским критериям III, более правомочным должен был быть диагноз «Синдром циклической рвоты» (CVS).
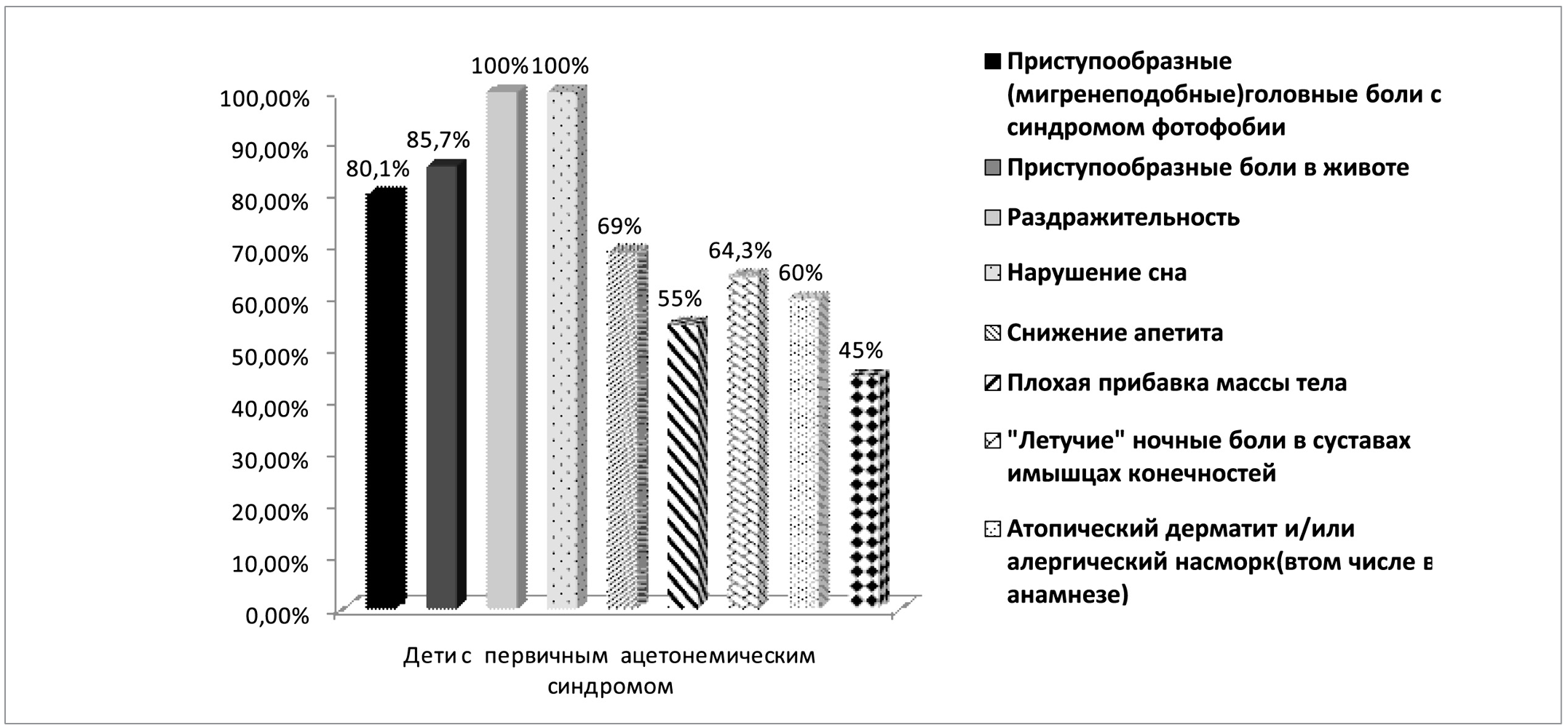
Рис.2. Клинические симптомы внеприступного периода у пациентов при первичном АСД (CVS).
Rice. 3. Особенности семейного анамнеза детей с первичным ацетонемическим синдромом (% встречаемости у членов семьи)
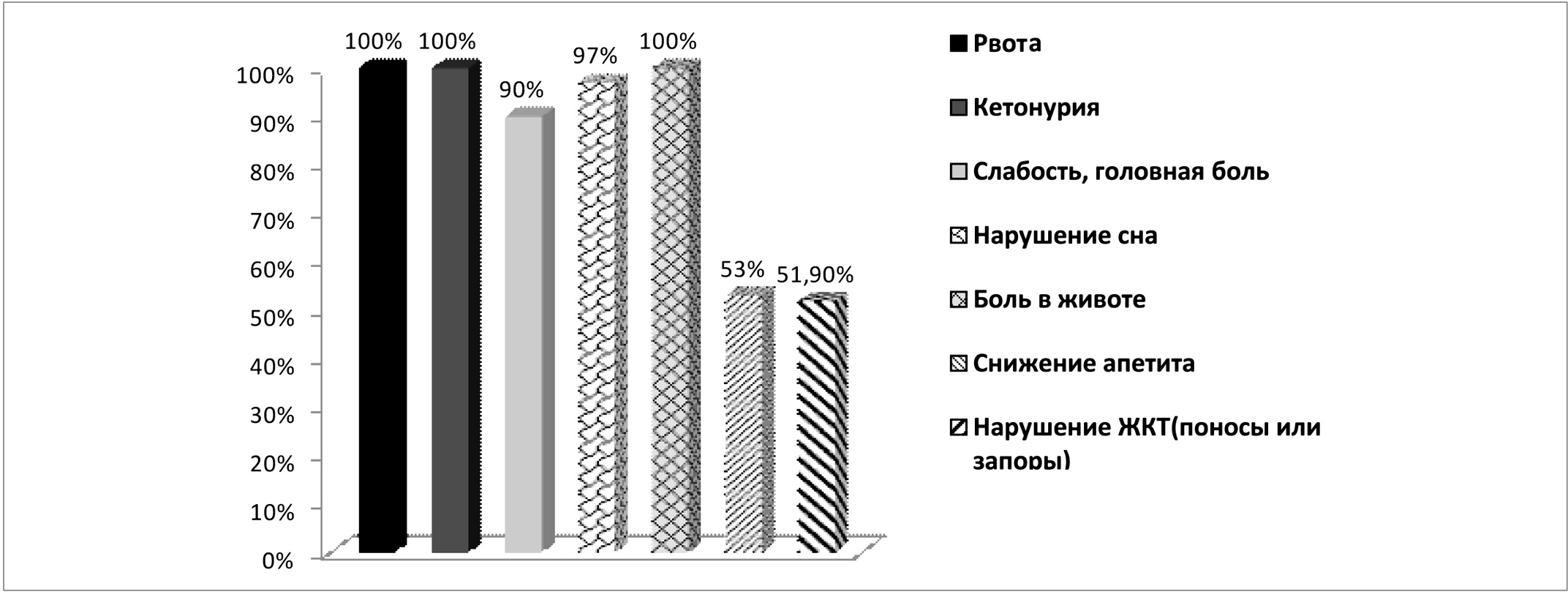
Rice. 4. Жалобы при АСД на момент начала заболевания
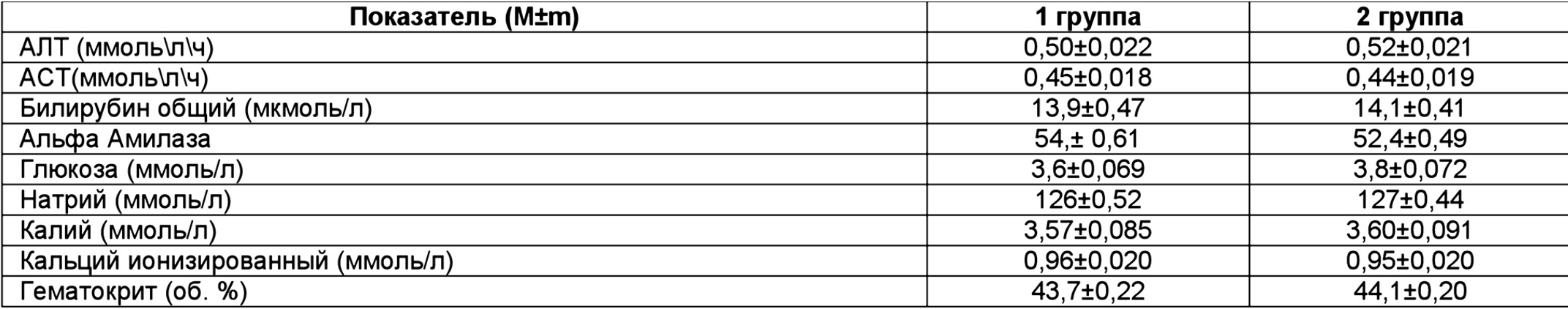
Table 2
Биохимические показатели у обследованных детей в начале возникновения ацетонемического синдрома
Учитывая, что такие изменения носят семейный характер, нами был детально проанализирован семейный анамнез в группе первичного АСД (всего 42 пациента). Особенности семейного анамнеза детей с первичным ацетонемическим синдромом представлены на рисунке 3.
Как видно из данных рисунка 3, факторы риска развития АСД были у всех детей с первичным АСД, что является одним из ведущих критериев ранней диагностики синдрома циклической рвоты (CVS) [11,12,13].
Данные, представленные на рисунках 2 и 3, должны быть тщательно проанализированы семейными врачами и педиатрами с целью ранней диагностики первичного АСД. Также следует обратить внимание на группы семейного риска («факторы риска») по развитию АСД с соответствующими режимными, диетическими и, при необходимости, медикаментозными рекомендациями.
Жалобы у всех обследованных детей на момент поступления представлены на рисунке 4.
Следует отметить, что параклинические показатели при поступлении в стационар или начале амбулаторного лечения в 1 и 2 группах были близки и статистически достоверно не отличались.
Результаты исследования биохимических показателей у детей всех групп в начале ацетонемического синдрома представлены в таблице 2.
Как видно из таблицы 2, в начале заболевания у детей всех групп отмечено снижение уровня натрия, калия, кальция плазмы крови, отмечено повышение уровня гематокрита. Это свидетельствует об электролитных потерях и изменениях ОЦК. Такие состояния являются основанием как для проведения регидратационной терапии, так и назначения препаратов детоксикационной направленности.
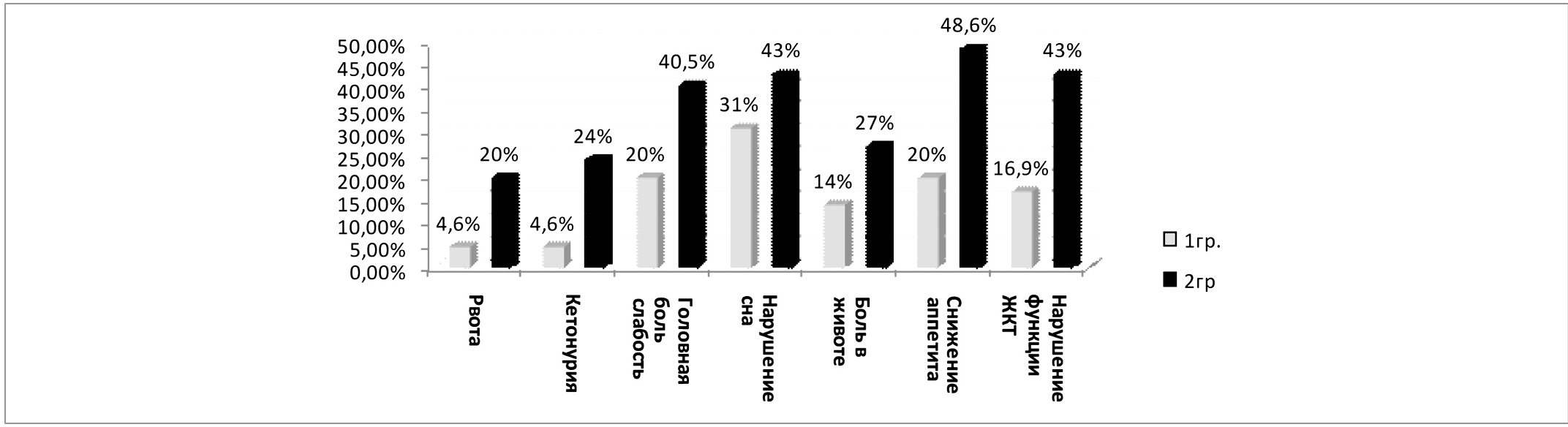
Rice. 5. Динамика основных клинических симптомов в процессе лечения (к 5 дню терапии)
Table 3
Динамика показателей электролитов крови у детей с ацетонемическим синдромом (5 день лечения)

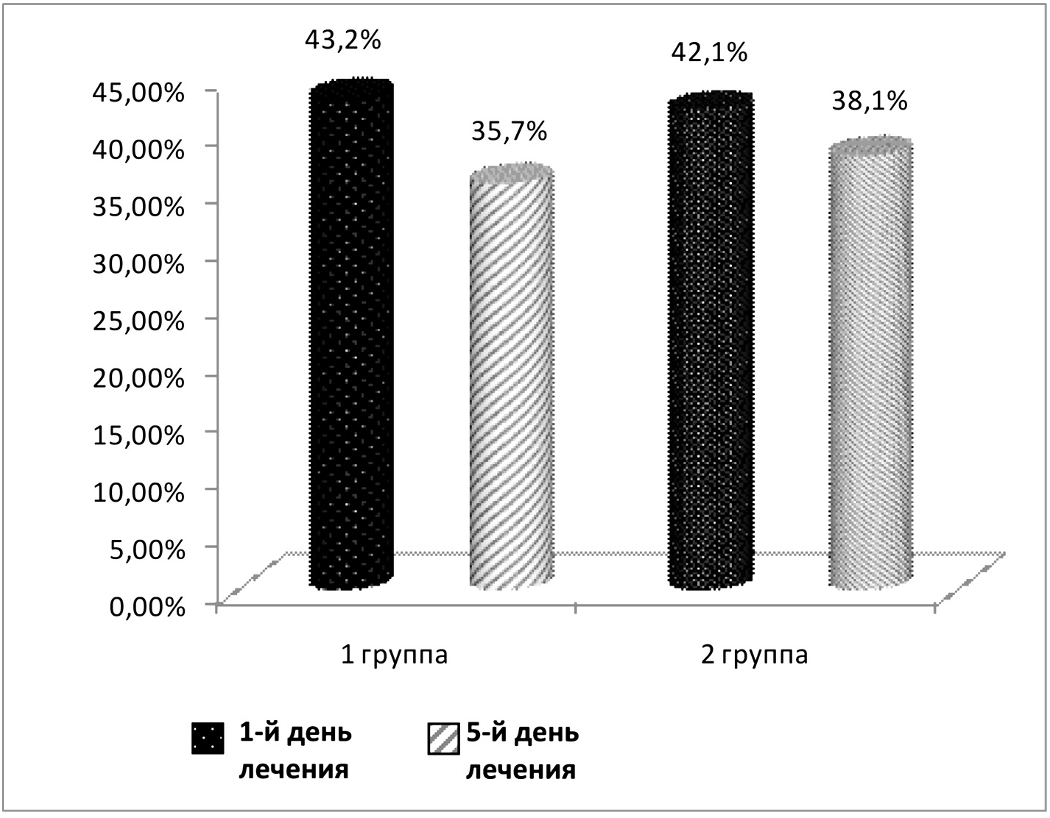
Rice. 6. Динамика показателей гематокрита у обследованных детей в процессе лечения (1 и 5 дни лечения)
Регидратационная терапия детям 1 группы была проведена раствором Регидрон Оптим, во 2 группе — другими регидратационными средствами. Детям 1 группы также сразу был назначен энтеросорбент 4 поколения Атоксил.
Длительность регидратационной терапии в комбинации с использованием энтеросорбента Атоксил в 1 группе составляла до 3-х дней у 70,8% (46 детей). К 5 дню все дети этой группы не нуждались в регидратационной терапии.
Во 2 группе регидратационная терапия на протяжении 3-х дней была проведена у 56,7% (21 детей), а к 5 дню лечения эффект был достигнут у 75,7% (28 детей) обследуемых.
Большинству детей (80% обследуемых) в первые трое суток лечения 1–2 раза в день делалась очистительная клизма с 1% раствором пищевой соды. При необходимости симптоматически вводились противорвотные и спазмолитические препараты. В первые дни лечения дети получали индивидуальное дробное кормление (перетертые супы, теплое сладкое питье, сухарики). В дальнейшем диетотерапия также соответствовала протокольным рекомендациям.
Все пациенты 1 группы хорошо переносили комбинированную терапию препаратами Регидрон Оптим и Атоксил. Об эффективности указанной терапии говорит отсутствие необходимости назначения в этой группе пациентов инфузионной терапии.
Во 2 группе показатель инфузионных вмешательств составил 32,4% (12 случаев), причем это лечение проводилось как при первичном, так и при вторичном АСД.
Динамика основных клинических симптомов в процессе лечения (в частности к 5 дню терапии) представлена на рисунке 5.
Как видно из данных рисунка 5, позитивная динамика в 1 группе существенно опережала аналогичные показатели пациентов группы 2 (во всех случаях p<0,05).
Динамика обследования пациентов в процессе лечения представлена в таблице 3 и на рисунке 6.
Как видно из данных таблицы 3 и рисунка 6, показатели электролитного обмена и гематокрита в процессе лечения у всех обследованных имели тенденцию к нормализации. Однако к 5 дню терапии эта позитивная динамика более четко прослеживается у пациентов 1 группы по сравнению со 2 группой.
Учитывая положительную динамику заболевания, 100% детей 1 группы были выписаны к 6 дню пребывания в стационаре. Средняя длительность пребывания в стационаре у детей 2 группы составила 7,9 койко-дня.
Conclusions
Таким образом, для медицинских работников и родителей очень важно определить характер АСД (первичный или вторичный), что позволит дифференцированно подойти к лечению и профилактике этих состояний. Для определения вида ацетонемического синдрома у детей весьма важен правильный сбор семейного анамнеза и детализация клинических особенностей межприступного периода.
Семейные врачи и педиатры должны обращать особое внимание на наличие в семье так называемых «факторов риска»: мигрени, мочекаменной или желчнокаменной болезни, подагры, сахарного диабета, ацетонемического синдрома в детстве у членов семьи, ожирения и/или артериальной гипертензии. Ибо полное или даже частичное сочетание этих «факторов риска» в семейном анамнезе у пациентов с АСД является одним из критериев ранней диагностики первичного ацетонемического синдрома (синдрома циклической рвоты — CVS).
Для своевременной диагностики первичного АСД очень важно обратить внимание на ведущие проявления внеприступного периода и анамнестические данные у ребенка: приступообразные (мигренеподобные) головные боли; приступообразные боли в животе; раздражительность, нарушение сна; снижение аппетита, плохая прибавка массы тела; «летучие» ночные боли в суставах и мышцах конечностей; склонность к атопическому дерматиту и/или аллергическому насморку, энурезу и/или логоневрозу (в том числе в анамнезе).
По нашим данным, наличие тех или иных указанных проявлений внеприступного периода и особенностей анамнеза, в том числе семейного, отмечено у всех пациентов с первичным ацетонемическим синдромом. Причем более чем у 80% детей зарегистрировано сочетание «факторов риска» по трем и более позициям, а у одной трети пациентов выявлена их 100% комбинация.
В лечении ацетонемического синдрома детей (как в продромальном, так и в приступном периоде) высокая эффективность достигается при раннем назначении регидратационной терапии с использованием препарата Регидрон Оптим в комбинации с энтеросорбентом 4 поколения — препаратом Атоксил.
Предложенный подход к проблеме ацетонемического синдрома у детей, который позволит семейным врачам и педиатрам своевременно заподозрить или диагностировать первичный ацетонемический синдром у детей (синдром циклической рвоты — CVS), включает: детализацию семейного анамнеза; детализацию анамнеза болезни и жизни у ребенка (по указанным критериям); адекватную оценку ведущих симптомов во внеприступном периоде.
Знание этих клинико-анамнестических показателей позволит своевременно и адекватно начать стартовую терапию ацетонемического синдрома у детей (как первичного, так и вторичного) с высокоэффективного регидратационного средства (Регидрон Оптим) в комбинации с энтеросорбентом 4 поколения (Атоксил).
Совокупность таких подходов даст возможность семейным врачам и педиатрам оптимизировать терапию такого распространенного состояния, как ацетонемический синдром у детей, и улучшить качество жизни у этих пациентов.
LITERATURE
- Ацетонемический синдром у детей — возможности оптимизации терапии / В. В. Корнева, В. В. Козачук, Л. Г. Курило [та ін.] // Суча- сна гастроентерол. — 2011. —№ 2. — С. 45—48.
- Бондарев Е. В. Применение энтеросорбентов в медицинской практи- ке [Электронный ресурс] / Е. В. Бондарев, С. Ю. Штрыголь, С. Б.Дырявый. — Х. : Национальный фармацевтический университет.— Режим доступа : http://www.provisor.com.ua. — Title from the screen.
- Ефективність ентеросорбційної терапії в комплексному лікуванні аскаридозу у дітей : інформ. лист. / В. В. Бережний, Т. В. Марушко, В. В. Корнєва[та ін.]. — К., — 4 с.
- Зубаренко А. В. Дисметаболические нефропатии в педиатриче- ской практике. Сообщение / А. В. Зубаренко, Т. В. Стоева // Здо- ровьеребенка. — 2009. — № 4 (19). — С. 22—25.
- Казак С. С. Діагностика та дієтотерапія ацетонемічного синдрому у дітей / С. С. Казак, Г. В. Бекетова // Ліки України. — —№ 1. — С. 83—86.
- Квашнина Л. В Нейро-артритическая аномалия конституции, нарушения пуринового обмена и ацетонемический синдром у детей / Л. В.Квашнина, Н. Б. Евграфова // Доктор. — — № 3. — С. 79—82.
- Курило Л. В. Ацетонемический синдром: болезнь или образ жизни? / Л. В. Курило // Здоровье Украины. — — № 10. — С. 34—35.
- Надрага О. Б. Ефективність застосування сорбенту «Атоксил» у комплексному лікуванні ротавірусних гастроентеритів у дітей раннього віку / О. Б.Надрага, Г. О. Литвин, Н. М. Поцілуйко // Совр. педиатрия. — 2011. — № 2. —С. 138—141.
- Оценка эффективности энтеросорбента Атоксил в комплексном лечении аскаридоза у детей / В. В. Корнева, Л. В. Курило, В. Г. Козачук [и др.]// Совр. педиатрия. — — № 3. — С. 62—65.
- Палий И. Г. Современный взгляд на проблему энтеросорбции: выбор оптимального препарата / И. Г. Палий, И. А. Резниченко // Нов. медицины ифармации. — — № 11 (217). — С. 15—17.
- Сапа Ю. С. Синдром циклической ацетонемической рвоты / Ю. С. Сапа [Электронный ресурс]. — Режим доступа : http://www.rekicen.ru/php/content.php?group=1&id=422. — Title from the screen.
- Сенаторова А. С. Ацетонемический синдром у детей / А. С. Сенаторова, Е. В. Осипенко // Здоровье ребенка. — — № 5 (8). — С. 42—46.
- Синдром циклічної блювоти. Протоколи діагностики та лікування захворювань органів травлення у дітей : наказ МОЗ України № 438 від05.2010 [Електронний документ]. — Режим доступу : http://www.moz.gov.ua. — Назва з екрану.
- Apical effect of diosmectite on damage to the intestinal barrier induced by basal tumor necrosis factor / Mahraoui, М. Heyman, О. Plique [еt al.] // Gut. —1997. — Vol. 40. — P. 339—343.
- Kim Y. Reduced osmolarity oral rehydration solution for treating dehydration due to diarrhea in children: systematic review / S. Y. Kim, P. Garner // BMJ. —2001. — Vol. 323. — P. 81—85.
- Recommendations for composition of oral regidratation solution from the children of Report of an ESPGAN working group
- Booth, R. Cunha Ferreira, J. F. Desjeux [et al.] // J. Pediatr. Gastroen- terol. Nutr. — 1992. — Vol. 14. — P. 113—115.
