Застосування методів сорбції при захворюванні печінки, асоційованих з дисбактеріозом кишечника у дітей раннього віку
УДК 616.36-053.36:615.246.2
О.Г. Шадрін, Н.Ф. Чернега
ДУ «Інститут педіатрії, акушерства та гінекології НАМН України», м. Київ
Резюме. В статті наведені результати ефективності застосування препарату «Атоксіл» у комплексному лікуванні дітей раннього віку з ушкодженням печінки, асоційованим з дисбіозом кишечнику.
Ключові слова: діти раннього віку, захворювання печінки, Атоксіл.
Вступ
Ураження печінки у дітей раннього віку є надзвичайно актуальною проблемою, що обумовлено, передусім, низькою ефективністю лікування та швидким прогресуванням фібротичних змін в даній віковій категорії.
Принцип лікування хвороб печінки передбачає два головні напрями: етіотропну і патогенетичну терапію. Етіотропна терапія застосовується при вірусних ураженнях і є суворо обґрунтованою і стандартизованою. Враховуючи її обмежене застосування і низьку ефективність при лікуванні у дітей раннього віку, важливим напрямком лікування є патогенетичний.
Гепатобіліарна система є основною сполучною ланкою між шлунково-кишковим трактом (ШКТ) та внутрішнім середовищем організму. ШКТ є першим функціональним бар’єром, який забезпечує всмоктування і концентрацію не тільки необхідних, але й шкідливих речовин, які включають і продукти життєдіяльності мікрофлори кишечнику. Дисбіотичні зміни в кишечнику належать до несприятливих факторів ушкодження печінки [3].
Нормальна мікрофлора в організмі виконує низку важливих функцій, серед яких є синтез вітамінів (В1, В2, В6, К, фолієва, нікотинова кислоти та ін.) і участь у процесах травлення. Компоненти їжі розщепляються широким спектром бактеріальних ферментів до олігомерів, які у свою чергу ферментуються до коротколанцюгових жирних кислот, органічних кислот та інших продуктів. Кінцеві компоненти гідролізу забезпечують трофіку слизової оболонки кишечнику, підвищують її енергетичний потенціал і стимулюють моторику. Важливою функцією кишкової мікрофлори є участь в активації місцевих і загальних імунних реакцій. Слизова оболонка кишечнику, маючи власну лімфоїдну систему, є одним з найбільш значущих компонентів імунної системи макроорганізму. Нормальна кишкова мікрофлора бере участь в активації імунних реакцій і формуванні імунної толерантності макроорганізму.
Дисбаланс мікрофлори кишечнику призводить до збільшення пропорції потенційно-патогенних грамнегативних бактерій, які продукують токсичні метаболіти. Використовуючи в якості харчового субстрату білок і продукти його гідролізу, патогенна мікрофлора викликає гнилісні процеси, кінцевими метаболітами яких є аміак, ароматичні амінокислоти, сульфіти, ендогенні токсини. Продукти такого обміну сприяють запаленню слизової оболонки, діареї, порушенню пристінкового травлення, підвищенню газоутворення. Накопичені в просвіті кишечнику ендотоксини патогенних бактерій проникають через слизову кишечнику в систему кровообігу і воротну вену і викликають ушкодження гепатоцитів. Анаеробними грамнегативними бактеріями факультативно вивільняється до 90% всіх ендотоксинів, які ушкоджують клітинні мембрани.
У дітей раннього віку ендотоксини досить швидко призводять до подразнення рецепторного апарату ентероцитів, змін ферментативної активності, секреції, всмоктування і, як наслідок, порушення мотрики ШКТ. Таким чином, порушення кишкового захисного бар’єру посилює навантаження на ферментні системи печінки і, за певних умов, сприяє метаболічним та структурним змінам в органі. В умовах патології виникає порочне коло дизметаболічних змін, яке сприяє накопиченню проміжних продуктів порушеного обміну речовин і ендотоксинів, що призводить до розвитку ендогенної інтоксикації. У зв’язку з цим, з точки зору клінічної фізіології, особливу актуальність в комплексній терапії ушкоджень печінки у дітей набувають методи детоксикації з використанням сорбційних препаратів.
Клінічна ефективність ентеросорбції при захворюваннях печінки обумовлена різними механізмами дії ентеросорбентів. Основний ефект реалізується прямою детоксикуючою дією по відношенню до токсичних метаболітів і токсинів кишкової мікрофлори, яка, за даними деяких повідомлень, має негативні зміни при захворюваннях печінки [1]. Важливим механізмом дії ентеросорбентів є вплив на ферментативну насиченість і концентрацію біологічно активних речовин в слизовій оболонці ШКТ, які визначають прояви диспепсії при захворюваннях гепатобіліарної системи. Окрім того, сорбенти мають властивість підвищувати, за рахунок концентраційних і осмотичних градієнтів, виведення ендотоксинів із внутрішньої середовища організму в порожнину кишечнику. Цей механізм визначає роль ентеросорбентів при ушкодженнях печінки, незалежно від їх етіології.
На сьогодні визначають декілька груп ентеросорбентів: вуглеводні, кремнійвмісні, природні органічні на основі харчових волокон, лігніну, пектинів, природних і синтетичних смол, синтетичних полімерів [4]. Одними із найбільш застосовуваних в педіатрії є кремнійвмісні сорбенти, зокрема Атоксіл. Суттєвою відмінністю сорбенту є непориста структура, відсутність якої забезпечує високу швидкість перебігу процесів абсорбції, максимум дії якої проявляється вже через 4 хвилини.
Атоксіл має білковозв’язуючі властивості, що надає йому здатність адсорбувати патогенні мікроорганізми із ШКТ і виводити із організму токсичні речовини різного походження, у тому числі алергенні мікробні ендотоксини. Атоксіл є вітчизняним препаратом і відповідає основним вимогам, які ставляться до сорбентів: нетоксичний, не травмує слизову оболонку ШКТ, легко евакуюється із ШКТ, має хороші сорбційні і органолептичні властивості.
Метою нашої роботи було вивчення ефективності застосування сорбенту Атоксіл в комплексній терапії дітей з ушкодженням печінки, асоційованим з дисбіозом кишечнику.
Матеріал і методи дослідження
Під нашим спостереженням знаходились 34 дитини віком від 1 до 3-х років з ураженням печінки, асоційованими з дисбіозом кишечнику.
Основну групу склали 14 дітей: 9 дітей з гепатитами інфекційної природи та криптогенні, 5 мали ушкодження, обумовлені порушеннями обміну (3 дитини з муковісцидозом, 1 — з глікогенозом, 1 — з целіакією).
Контрольну групу склали 20 хворих з ушкодженням печінки, порівнянні за віком, які проходили лікування в нашому відділенні без включення в терапію будь-яких сорбентів.
Обстежені діти отримували стандартне комплексне лікування із застосуванням противірусних засобів, гепатопротекторів, пробіотиків, вітамінів, а діти основної групи — препарат Атоксіл. Препарат застосовувався із розрахунку 150 мг/кг маси тіла на добу, призначався за 1 годину до або через 2 години після їжі, тричі на день.
Рекомендовані дози Атоксілу: у дітей 1–2 років добова доза становить 2 г, 2–4 років — 3 г, 4–7 років — 4 г, 7–12 років — 5–6 г, старше 12 років — 8 г. Інші медикаменти приймались через 2 години після прийому сорбенту. Курс лікування становив 14 днів.
Результати дослідження та їх обговорення
Клінічна симптоматика у обстежених дітей характеризувалась специфічними клініко-лабораторними проявами: гепато- і спленомегалією, диспептичним і геморагічним синдромами, збільшенням рівня трансаміназ. Основним проявом, за даними фізикального обстеження, була гепатомегалія (85,7% дітей основної групи і 85,0% дітей контрольної групи), стабільно тривала за період спостереження, ступінь проявів не завжди відповідав ступеню важкості захворювання. При високій активності процесу збільшення печінки супроводжувалося змінами її консистенції. Гепатомегалія супроводжувалась збільшенням селезінки у 35,7% дітей основної і 30,0% дітей контрольної групи. Геморагічний синдром зустрічався при активному процесі (21,4% дітей основної і 15,0% контрольної груп), був супутнім при важкому перебігу гепатиту, характеризувався кровоточивістю з місць ін’єкцій, появою геморагій на шкірі та слизових оболонках.
Характерними біохімічними змінами у крові для хворих на гепатити різної етіології були: тривала гіпербілірубінемія, переважно за рахунок кон’югованого білірубіну, стійке підвищення печінково-клітинних ферментів (АЛТ, АСТ, ЛДГ, ГГТ та інших); підвищення глобулінових фракцій, зниження альбумінів та факторів згортання крові (протромбіну, фібриногену та інших). Активність трансаміназ корелювала із важкістю перебігу. Активність процесу оцінювалася за концентрацією трансаміназ. Мінімальна активність характеризувалась підвищенням трансаміназ до 1,5–2 норм, низька — до 3–5 норм, помірна — до 9 норм і висока — вище 10 норм. Нормальний рівень трансаміназ за відсутності патологічних змін з боку інших біохімічних показників, які характеризують функціональний стан печінки, розцінювався як неактивний процес. Серед обстежених дітей превалювали малоактивні форми захворювання (57,1% дітей основної і 60,0% контрольної груп). Такому перебігу гепатиту відповідала досить слабко виражена клінічна симптоматика. Помірна та висока активність процесу відмічена у 42,9% і 40,0% обстежених дітей відповідно.
Ознаки холестазу у вигляді жовтяниці шкіри і слизових, епізодів ахолічного стільця спостерігались у 57,1% дітей основної і 60,0% дітей контрольної груп, хоча його класичних проявів у вигляді стійкого свербежу у обстежених дітей не спостерігалось. Диспептичний синдром, який реєструвався за рахунок функціональних порушень ШКТ (порушення апетиту, метеоризм, розлад випорожнень), виявлено у 92,0% дітей основної і 90,0% дітей контрольної груп. В клінічній картині обстежених дітей домінували інтоксикаційні порушення. Інтоксикаційний синдром спостерігався у всіх хворих і характеризувався блідістю, млявістю, поганим апетитом, втратою маси тіла, м’язовою гіпотонією, гіпорефлексією, здуттям живота. У частини дітей відмічалась низька динаміка збільшення маси тіла. В цілому клінічна картина хвороби, за винятком гепатомегалії, характеризувалася виразною лабільністю клінічних симптомів. Загальний стан дітей в більшості випадків реєструвався як середньої важкості і спостерігався у 64,2% дітей основної та 70,0% дітей контрольної груп.
Критеріями ефективності лікування були динаміка основних клінічних проявів (інтоксикації і диспептичних порушень) та лабораторних показників мікробіологічного дослідження випорожнень. Відповідно до розробленого протоколу спостереження наявність і ступінь проявів основних клінічних симптомів оцінювались за бальною шкалою (2 — виражений симптом, 1 — слабо виражений, 0 — симптом відсутній) до початку лікування, на 7-й і 14-й дні спостереження. Під час аналізу тривалості об’єктивних проявів хвороби враховувались порушення загального стану та роздратованість дитини як прояви інтоксикаційного синдрому.
У всіх обстежених хворих мали місце клінічні прояви дисбактеріозу і проявлялись зниженням апетиту, метеоризмом, кишковими коліками, змінами характеру випорожнень. Бактеріологічне дослідження калу проводилось класичним методом, для оцінки стану мікробіоценозу кишечнику визначали кількість бактерій у фекаліях шляхом засіву серійних розведень на диференційно-діагностичні середовища (Методичні рекомендації №10-13/3114/1U 1986 р.). Дисбіоз оцінювали відповідно до класифікації І.Б. Куваєвої і К.С. Ладодо (1991) [2].
Перший ступінь — латентна фаза дисбіозу. Зниження на 1–2 порядки кількості біфідобактерій (ББ), лактобактерій (ЛБ), а також повноцінних кишкових паличок до 80% від загальної кількості. Інші показники відповідають фізіологічній нормі (еубіозу). Клінічних проявів дисбіозу в цій фазі немає.
Другий ступінь — пускова фаза. Характеризується виразним дефіцитом ББ на фоні нормальної або зниженої кількості ЛБ або зниження їх кислотопродукуючої активності, дисбалансом в кількості і якості кишкових паличок, серед яких зростає доля лактозонегативних або цитратасимілюючих варіантів. Зростає кількість або плазмокоагулюючих стафілококів, або протеїв, або грибів роду Candida. Функціональні порушення травлення виражені нечітко — спорадичний рідкий стілець зеленуватого кольору, зі зсувом pH в кислий бік, іноді затримка випорожнень.
Третій ступінь — фаза агресії аеробної флори. Збільшення агресивних мікроорганізмів: стафілокок золотистий, протей, гемолітичні ентерококи; спостерігається заміщення повноцінних ешерихій бактеріями роду Klebsiella, Enterobacter, Citrobacter та ін. Функціональні порушення кишечнику у вигляді порушень моторики, секреції ферментів та всмоктування.
Четвертий ступінь — фаза асоціативного дисбіозу, характеризується глибоким розбалансуванням кишкового мікробіоценозу зі змінами кількісного співвідношення основних груп мікроорганізмів, зміною їх біологічних властивостей, накопиченням токсичних метаболітів.
Таблиця 1
Частота порушень мікробного спектру товстої кишки у дітей з ушкодженням печінки

Таблиця 2
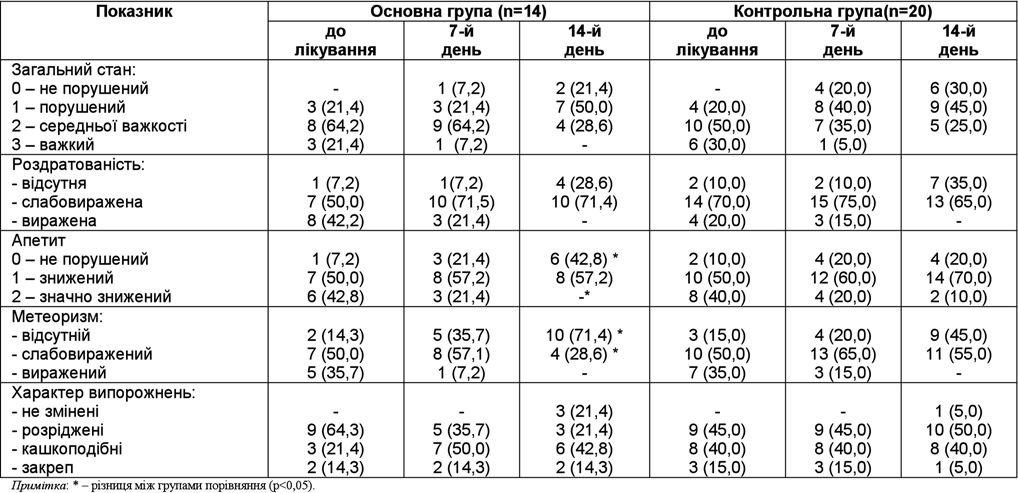
Динаміка клінічних симптомів у обстежених дітей в процесі лікування, абс/%
Характерно вегетування ентеропатогенних серотипів E. coli, сальмонел, шигел та інших збудників гострих кишкових інфекцій. Можливе розмноження клостридій.
При аналізі мікробіологічних досліджень випорожнень виявлено зміни у хворих обох груп (табл. 1).
Характеристика мікробного пейзажу у дітей з ушкодженням печінки проявлялася дефіцитом біфідо- (<109 КУО/г) і лактобактерій (<107 КУО/г), підвищенням кількості та зміною видового співвідношення умовно-патогенних бактерій. Так, серед дітей встановлено вірогідне пригнічення біфідобактерій (57,1% дітей основної групи і 70,0% дітей контрольної), лактобактерій (64,2% і 55,0% відповідно), кишкової палички (57,1% і 30,0% відповідно); її ферментативні властивості були змінені у 42,8% і 50,0% відповідно. Кількісне зниження супроводжувалося збільшенням питомої ваги умовно-патогенної флори: Klebsiela pn, S. аureus, ентерококів. У дітей обох груп (21,4% дітей основної групи і 15,0% контрольної) встановлена асоціація кількох видів умовно-патогенних мікроорганізмів у різних комбінаціях. У дітей обох груп виявлено порівнянні зміни складу кишкової мікрофлори, ступінь дисбактеріозу не мала суттєвих розбіжностей.
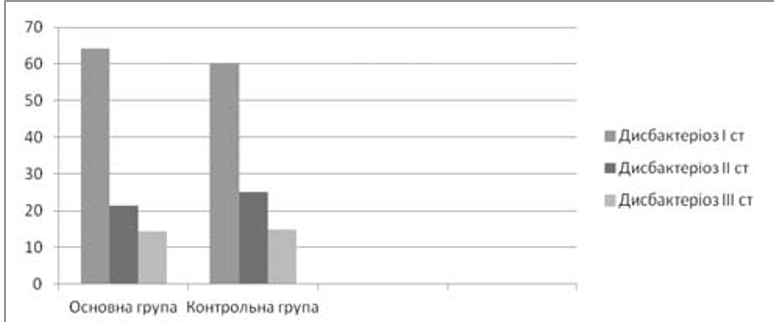
Рис. 1. Розподіл хворих дітей за ступенем дисбактеріозу на початку спостереження, %

Рис. 2. Розподіл хворих дітей за ступенем дисбактеріозу на 14-й день спостереження, %
Так, в основній групі дисбактеріоз I та II ступеня реєстрували у 9 (64,2%) і 3 (21,4%) дітей, у 2 (14,3%) випадках спостерігався дисбіоз III ступеня. В контрольній групі дисбактеріоз I ступеня виявлено в 60,0%, II — в 25,0%, III — в 15,0% випадків (рис. 1).
Аналіз динаміки клінічних симптомів показав ефективність лікування в обох групах. Під час аналізу тривалості об’єктивних проявів (інтоксикаційного та диспептичного) було виявлено зміни між групами порівняння за показниками апетиту та здуття живота. Динаміка клінічних симптомів перебігу захворювань наведена в таблиці 2.
Темп нормалізації диспептичних проявів у вигляді метеоризму та порушення апетиту на 7-й день лікування був однаковим в обох групах хворих, а на 14-й день відмічено достовірне підвищення у дітей основної групи (42,8% дітей основної групи проти 20,0% дітей контрольної); зникнення метеоризму мало місце у 71,4% хворих основної групи та лише у 45,0% дітей контрольної.
Також мало місце покращання характеристик випорожнень в основній групі: на 14-й день відмічено покращання у 42,8% дітей основної групи, а в контрольній — лише у 15,0% дітей. Слід зазначити, що у 2 дітей, які мали випорожнення кишечнику із схильністю до закрепів, характер стільця на фоні застосування Атоксілу не змінився.
Діти основної групи, які приймали Атоксіл протягом 2 тижнів, як свідчить проведений клінічний аналіз, мали суттєві зміни клінічних ознак дисбактеріозу (здуття живота, характер випорожнень). При мікробіологічному контролі випорожнень встановлено, що у 42,8% обстежених хворих після лікування із застосуванням Атоксілу відбулася нормалізація мікробіоценозу кишечнику, а в контрольній групі — лише у 15,0% випадків (р<0,05) (рис. 2).
Як видно з наведених даних, серед дітей, які приймали Атоксіл, у 42,8% відбулася повна нормалізація мікрофлори, а серед дітей, у яких дисбіотичні зміни залишились, їх виразність значно зменшилась: більшість із них (75%) мали дисбіотичні зміни І ступеня, не відмічено хворих з дисбактеріозом ІІІ ступеня.
В групі дітей, у яких не застосовувався сорбент, контрольні показники були достовірно нижчими: нормалізація мікрофлори відмічена лише у 15,0%, а серед дітей з дисбіотичними змінами у 52,9% спостерігався дисбактеріоз I ступеня, у 41,2% — II ступеня, у 1 дитини залишились дисбіотичні зміни ІІІ ступеня.
Кількісна оцінка мікробної флори у дітей обох груп дозволила встановити суттєве зниження контамінації кишок умовно-патогенною флорою: в основній групі її підвищення реєструвалось тільки у 3-х дітей. В групі порівняння достовірних змін не виявлялось.
Висновки
Порівняльний аналіз ефективності лікування дітей з ушкодженням печінки свідчить про достовірно швидшу динаміку усунення дисбіозукишечнику при застосуванні Атоксілу. Результати досліджень свідчать про доцільність його застосування в комплексному лікуванні хворих дітей зушкодженням печінки будь-якої етіології, асоційованим з дисбіозом кишечнику. Переносимість препарату задовільна, в процесі застосування не було відмічено жодного випадку непереносимості або побічної дії.
ЛIТЕРАТУРА
- Денисова М. Ф. Применение пробиотика лактив-ратиофарм в комплексном лечении хронических вирусных гепатитов у детей / М. Ф. Денисова, Н. Н. Музыка, Т. А. Лысяная // Совр. педиатрия. — № 6 (28).
- Куваєва І. Б. Мікроекологічні і імунні порушення і дітей / І. Б. Куваєва, К. С. Ладодо. — М.,
- Кучеренко Н. П. Мікробіоценоз товстої кишки у хворих на вірусний гепатит / Н. П. Кучеренко, А. І. Бобровицька, І. О. Верещагін // Матеріали наук.—практ. конф. і пленуму асоціації інфекціоністів України. — Тернопіль, 2004. — С. 115—116
- Энтеросорбция: состояние вопроса и перспективы на будущее / Николаев В. Г., Михаловский С. В., Николаева В. В. [и др.] // Вісн. проблем біології імедицини. — Вип. 4. — С. 7—17.
