УДК 616.521-053.2.085+615.454.1
СТУПЕНЧАТАЯ ЭНТЕРОСОРБЦИЯ КАК ОПТИМАЛЬНЙ МЕТОДКОРРЕКЦИИ МИКРОБИОЦЕНОЗА КИШЕЧНИКА У БОЛЬНЫХ АЛЛЕРГОДЕРМАТОЗАМИ
Я.Ф. Кутасевич, И.А. Олейник, С.К. Джораева,В.Ю. Мангушева
ГУ «Институт дерматологи и венерологии НАМН Украины»
Резюме. В статье приводятся данные о терапевтической эффективности ступенчатой энтеросорбции с применением атоксила и элиминаль-геля у больных аллергодерматозами, учитывая исследование общего состояния, субъективных и объективных жалоб и микробиоценоза кишечника до и после проводимой терапии.
Ключевые слова: аллергодерматозы, микрофлора кишечника, дисбактериоз, ступенчатая энтеросорбция.
ВВЕДЕНИЕ
Согласно данным ВОЗ, аллергические заболевания (АЗ) занимают третье место в мире после сердечно-сосудистой и онкологической патологий. В Украине распространенность АЗ также продолжает возрастать, особенно среди населения промышленно развитых регионов. [1].
Одной из причин АЗ считается большая антигенная нагрузка на организм вследствие сочетанного воздействия природных и антропогенных факторов, в частности техногенных загрязнителей.
Кроме экзогенных факторов, исследователи выделяют и эндогенные факторы риска развития гиперчувствительности организма, в первую очередь отягощенную наследственность. Известно, что 40 % людей имеют наследственную склонность к атопии, и этот контингент населения особо чувствителен к неблагоприятным условиям окружающей среды. Со временем у этих лиц формируются АЗ с повышенным уровнем IgE, т.е. атопические АЗ. Часто наблюдается сочетанное воздействие нескольких факторов на организм: неблагоприятной экологической ситуации, профессиональной вредности, социальных условий и т.д., от которого прежде всего страдают пациенты с наследственной предрасположенностью. [12].
Значительную роль в формировании аллергии играют сопутствующие заболевания печени, почек, пищеварительного канала, дыхательной системы, кожи и пр. Анализ физического статуса аллергологических больных показал высокий процент (67,5 %) сопутствующей патологии, особенно патологии печени (хронические гепатохолециститы, желчекаменная болезнь, дискинезия желчевыводящих путей), почек. Эти заболевания играют немаловажную роль в патогенезе рецидивов АЗ как с иммунологическим механизмом развития, так и без такового. [3].
Особое внимание стоит уделить поражению ЖКТ у пациентов с аллергодерматозами. Практически в 100 % пациентов наблюдаются различные нарушения со стороны желудочно-кишечного тракта. Более чем у половины обследуемых встречается дискинезия желчных путей, у трети – гастродуодениты и панкреатиты, практически у всех больных АЗ при обследовании выявляются изменения со стороны микробиоценоза кишечника. [9].
Кроме нарушений микрофлоры кишечника у пациентов с аллергическими заболеваниями изменяется состав микрофлоры кожи, что приводит к ухудшению кожного процесса, присоединению бактериальной и микологической инфекции [2].
Существует два типа нарушений микробиоценоза кишечника: первый тип характеризуется снижением количества нормальной кишечной микрофлоры. Нарушается барьерная функция ЖКТ, вследствие истончения биопленки, на 95% состоящей из бифидобактерий. Снижение количества бифидобактерий приводит к развитию третьей степени тяжести дисбиоза, независимо от количества других представителей нормофлоры. Возникает пищевая сенсибилизация. При втором типе дисбиоза в слизистую оболочку, а затем в системный кровоток поступает большое количество инфекционных антигенов. В результате увеличивается количество условно-патогенной флоры, что способствует сенсибилизации и ухудшению течения кожного процесса. [4,5].
Одним из оптимальных, простых и физиологичных методов купирования токсикозов, связывания и элиминации является энтеросорбция. Данный метод эфферентной терапии направлен на лечение интоксикационного синдрома при различных заболеваниях, основанный на способности энтеросорбентов связывать и выводить из организма различные экзогенные вещества, микроорганизмы и их токсины, эндогенные промежуточные и конечные продукты обмена, способные накапливаться или проникать в полость желудочно-кишечного тракта в ходе течения патологического процесса. [11]
В основе метода сорбционной детоксикации организма лежат научно обоснованные четыре механизма снижения системной концентрации токсических веществ и метаболитов. Первый – предполагает возможность обратного пассажа токсических веществ из крови в кишечник с дальнейшим их связыванием на сорбентах (сходен с механизмом кишечного диализа). Второй – сводится к очистке пищеварительных соков ЖКТ, содержащих значительное количество токсичных веществ. Третий – заключается в модификации липидного и аминокислотного спектров кишечного содержимого (за счет избирательного поглощения сорбентом свободных жирных кислот). Четвертый – сводится к удалению токсических веществ, образующихся в самом кишечнике, восстановления целостности и проницаемости слизистых оболочек и снижения функциональной нагрузки на печень, что позволяет более полно использовать ее детоксикационный потенциал для смягчения проявлений системного токсикоза и улучшению функционального состояния ЖКТ в целом. При использовании при данной патологии энтеросорбенты (ЭС) достигается выведение аллергенов, медиаторов аллергии и широкого спектра веществ, участвующих в иммунных реакциях. [6,7-13].
Целью исследования являлось изучение терапевтической эффективности ступенчатой энтеросорбции с применением атоксила и элиминаль-геля.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование было включено 30 пациентов с аллергодерматозами в возрасте от 17 до 67 лет (17 мужчин и 13 женщин – 56,7 % и 43,3 % соответственно). Согласно клиническим и анамнестическим данным, хроническая экзема была выявлена у 7 (23 %) пациентов, аллергический дерматит у 6 (20%) пациентов, микробная экзема у 6 (20 %), атопический дерматит у 5 (17 %), токсикодермия у 4 (13%), крапивница у 2 (7 %) обследованных (рис.1).
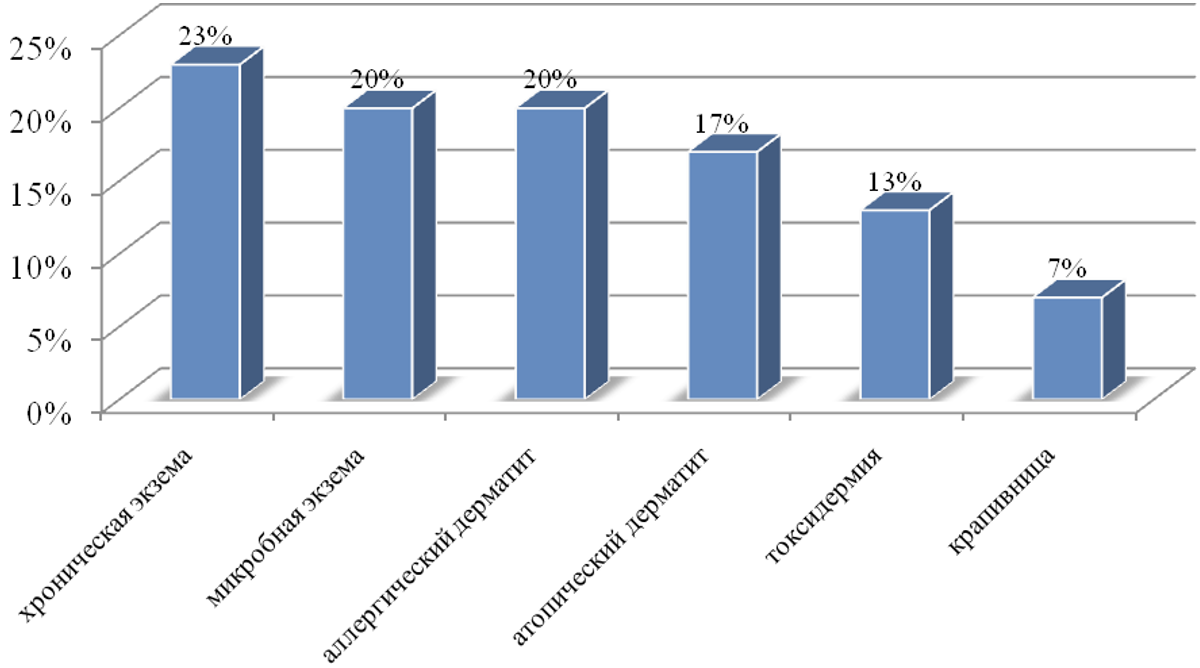
Рис. 1. Раcпределение больных по нозологическим формам
Диагноз устанавливали на основании жалоб, анамнестических данных, клинической картины, результатам объективного обследования. Всем больным в начале и конце лечения проводились лабораторные исследования (общий анализ крови, мочи, биохимический анализ крови с определением глюкозы, общего белка, общего билирубина и его фракций, АЛТ, АСТ, микробиологическое исследование кала).
Микробиологическое исследование кала было проведено на базе бактериологической лаборатории областной СЭС г. Харькова, лаборатория аттестована на проведение данных исследований (свидетельство об аттестации № 100-163/2013 от 06.06.2013 года, действительное до 05.06.2016) и имеет разрешение на работу с возбудителями ІІІ-ІV групп патогенности (№ 130/28-12 от 21.12.2012, действительное до 21.12.2017).
Бактериологическое исследование кала и степень дисбиотических нарушений оценивалось согласно унифицированной рабочей классификации Куваевой-Ладодо. [13]. Выраженность проявлений дисбактериоза кишечника оценивали путем посева серийных разведений фекалий [14], с использованием плотных и жидких питательных сред: Эндо, Плоскирева, Сабуро, Симмонса, Олькеницкого, Вильсона-Блера, Блаурокка и др.
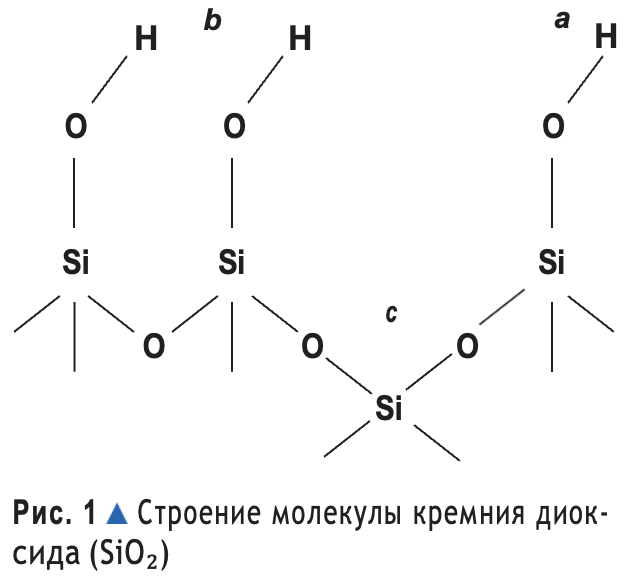
Атоксил – высокоактивный кремниевый сорбент IV поколения с площадью активной поверхности абсорбции более 400 м²/г, усиливает транспорт пищевых и бактериальных аллергенов, разнообразных токсических продуктов, в том числе средних молекул, олигопептидов, аминов и других веществ, образующихся в процессе гниения белков в кишечнике, из внутренних сред организма (крови, лимфы, интерстиция), в пищеварительный тракт за счет концентрационных и осмотических градиентов с последующим их выведением из организма. В 90-х годах прошлого века были обнаружены уникальные свойства атоксила. Атоксил обладает электростатической способностью сорбции, благодаря которой препарат, растворяясь в воде, приобретает отрицательный заряд и, соответственно, притягивает все, что положительно заряжено. Однако полезная микрофлора, витамины и микроэлементы, имеющие нейтральный заряд, им не сорбируются. Кроме того, данный препарат инактивирует большую белковую молекулу в сравнении с другими энтеросорбентами.
Элиминаль гель – комбинированный препарат, содержит в своем составе высокоактивный кремниевый сорбент и синтетический дисахарид лактулозу. Препарат обладает противомикробным действием, оказывает опосредованное дезинтоксикационное, бактерицидное и бактериостатическое действие по отношению к патогенным и условно патогенным бактериям и грибам. Оказывает направленное действие на выведение патогенных бактерий и энтеротоксинов, позволяет восстановить микробиоценоз кишечника и стимулировать рост и развитие нормофлоры – бифидо- и лактобактерий. Компоненты препарата обладают взаимодополняющим и усиливающим действием при коррекции состояний, связанных с нарушениями функционирования желудочно-кишечного тракта.
Для оценки терапевтической эффективности ступенчатой абсорбции все обследованные больные были разделены на две группы. Больные I группы получали традиционное лечение и ступенчатую терапию: атоксил по 1 флакону в день в течение 3 дней с последующим приемом элиминаль геля по 1 стик-пакету 3 раза в день в течение 14 дней; больные II группы – традиционное лечение без применения энтеросорбции.
Оценка терапевтической эффективности предложенной ступенчатой схемы энтеросорбции включала в себя динамику данных субъективных (жалобы на зуд, жжение, сухость) и объективных обследований (кожный процесс, а также в динамике изучалось состояние микрофлоры кишечника).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
В основной группе на фоне применения этапной схемы применения атоксила и элиминаль-геля улучшение общего состояния в контрольной группе отмечалось на 2–4 сутки, на фоне лишь базовой терапии в группе сравнения – на 7 сутки. Полный регресс кожного процесса в основной группе был отмечен на 9–11 день, в группе сравнения – на 14–17 день.
После проведенной терапии у больных основной группы отмечалось уменьшение зуда на 3–4 дня раньше, нежели в группе сравнения.
Наиболее выраженный терапевтический эффект наблюдался у больных токсидермией. Эту группу составили пациенты, страдающие алиментарной, реже медикаментозной токсидермией легкой и средней степени тяжести. Регресс высыпания отмечался на 2–3-и сутки, что было на двое суток раньше, нежели у пациентов группы сравнения.
У больных экземой (микробной и истинной) отмечался регресс островоспалительных высыпаний, уменьшение площади очагов поражения на 2–3 дня раньше, чем в группе сравнения.
В результате проведенных исследований до лечения нарушение микробиоценоза толстого кишечника было выявлено у всех 30 человек (100,0 %). Так, дисбактериоз I степени был выявлен у 3 (10,0 %), II степени – у 16 (53,3 %), III степени – 11 (36,7 %) обследованных лиц.
Дисбиотические нарушения характеризовались снижением количественного содержания индигенной микрофлоры – представителей как аэробных, так и анаэробных бактерий. Наиболее часто у пациентов отмечалось снижение количества бифидобактерий – у 9 (30 %) человек. Кроме этого, было отмечено снижение показателей высеваемости лактобактерий у 4 (13,3 %) больных и нормальной кишечной палочки у 3 (10 %) пациентов. Данные показатели заслуживают внимания, поскольку именно эти микроорганизмы, с одной стороны, обеспечивают колонизационную резистентность кишечного биотопа, препятствуя проникновению и закреплению на слизистой патогенных агентов; а с другой, они представляют собой природные биосорбенты, препятствующие всасыванию аллергенов в кишечнике и стимулирующие синтез Ig A – основных антител против пищевых аллергенов.
У 25 (83,3 %) больных было выявлено увеличение количества условно-патогенных микроорганизмов (H. alvei, K. pneumoniae, Proteus spp., E. aerogenes). На фоне качественного дисбаланса микрофлоры также были выявлены изменения количественного состава: у 9 (30,0 %) обследованных была выявлена кишечная палочка с гемолитическими свойствами, лактозоотрицательная – у 6 (20,0 %) и кишечная палочка со сниженной ферментативной активностью у 2 (6,7 %) больных. Обращает на себя внимание частота выявления грибов рода Candida и S. aureus – у 22 (73,3 %) и 4 (13,3 %) обследованных соответственно. Таким образом, выявленные нарушения колонизационной резистентности кишечного биотопа, связанные с изменением состава постоянной микрофлоры, способствуют его заселению патогенными и условно-патогенными микроорганизмами, что и приводит к формированию дисбиоза и, как следствие, к усилению пищевой сенсибилизации.
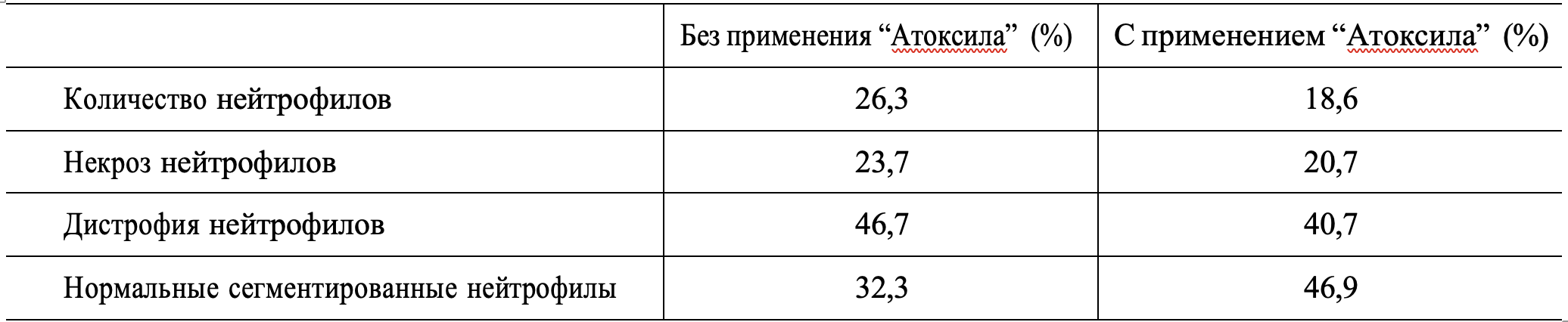
При микробиологическом исследовании кала основной группы (15 человек) после проведенного лечения была отмечена стойкая тенденция в нормализации основных показателей биоты кишечника. Так, дисбактериоз I степени был выявлен у 2 (13,3 %), II степени – у 6 (40,0 %), III степени – 2 (13,3 %) обследованных (до лечения 10,0 %, 53,3 % и 36,7 % соответственно); у 5 человек (33,3 %) на фоне проводимой терапии отмечалась полная нормализация всех показателей. Также у пациентов данной группы отмечалась нормализация содержания лакто- и бифидобактерий – 14 человек (93,3 %), у всех 15 пациентов восстановилось общее количество типичных кишечных палочек при полном отсутствии гемолизирующих кокков и условно-патогенных форм энтеробактерий. Также после проведенной комплексной терапии наблюдалось снижение показателей обсемененности грибами рода Candida с 73,7 % до 26,7 %.
При бактериологическом исследовании кала у пациентов группы сравнения (15 человек) положительные сдвиги в биоте кишечника были выражены значительно меньше. Дисбактериоз I степени был выявлен у 4 (26,6 %), II степени – у 10 (66,7 %) пациентов, III степени – 1 (6,7 %) обследованного. В основном сохранялось снижение содержания бифидобактерий (у 33,3 % обследованных), лактобактерий (13,3 % пациентов), типичной кишечной палочки (6,7 % больных) и повышение содержания кишечной палочки с гемолитической активностью (40,0 %), лактозонегативных форм (13,3 %) на фоне выявления кишечной палочки со сниженной ферментативной активностью (6,7 %), а также условно-патогенных микроорганизмов (53,3 %), кокковых форм бактерий (S. aureus – 6,7 %) и наличием грибов рода Candida (53,3 %). Таким образом сохранялась необходимость дополнительной коррекции биотопа клинически.
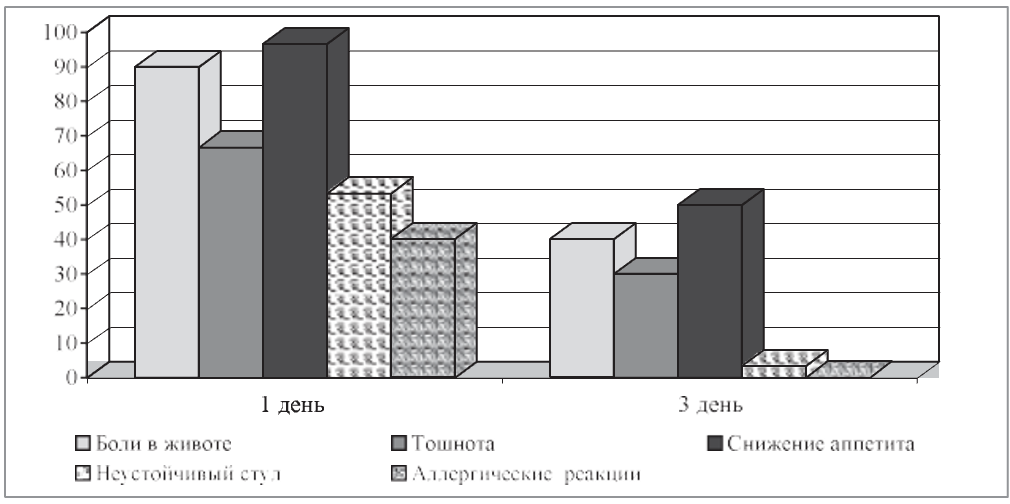
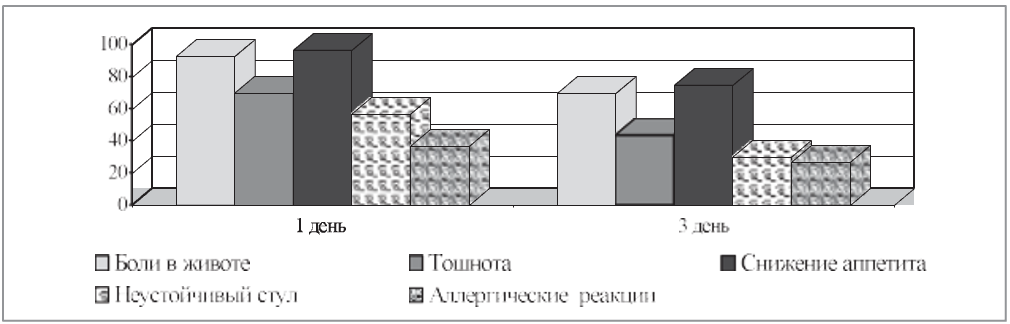
На следующих диаграммах представлена динамика основных показателей, характеризующих состояние ценоза кишечника до и после проведенной терапии (рис. 2, 3).
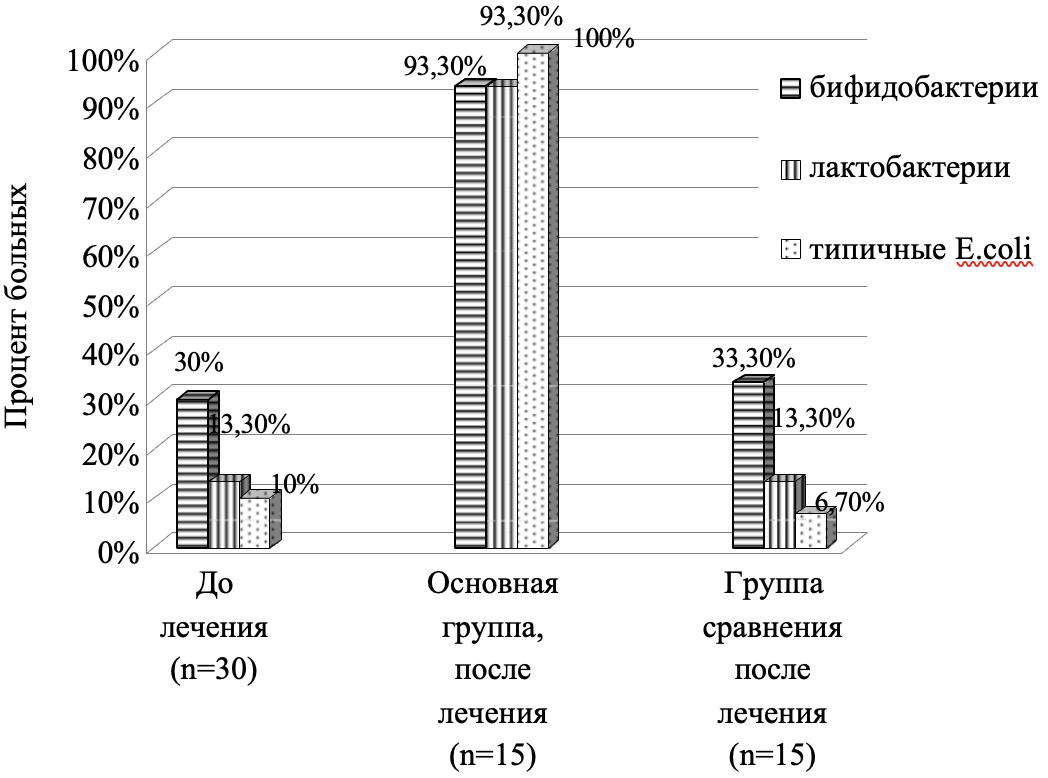
Рис. 2. Динамика основных показателей биоты кишечника
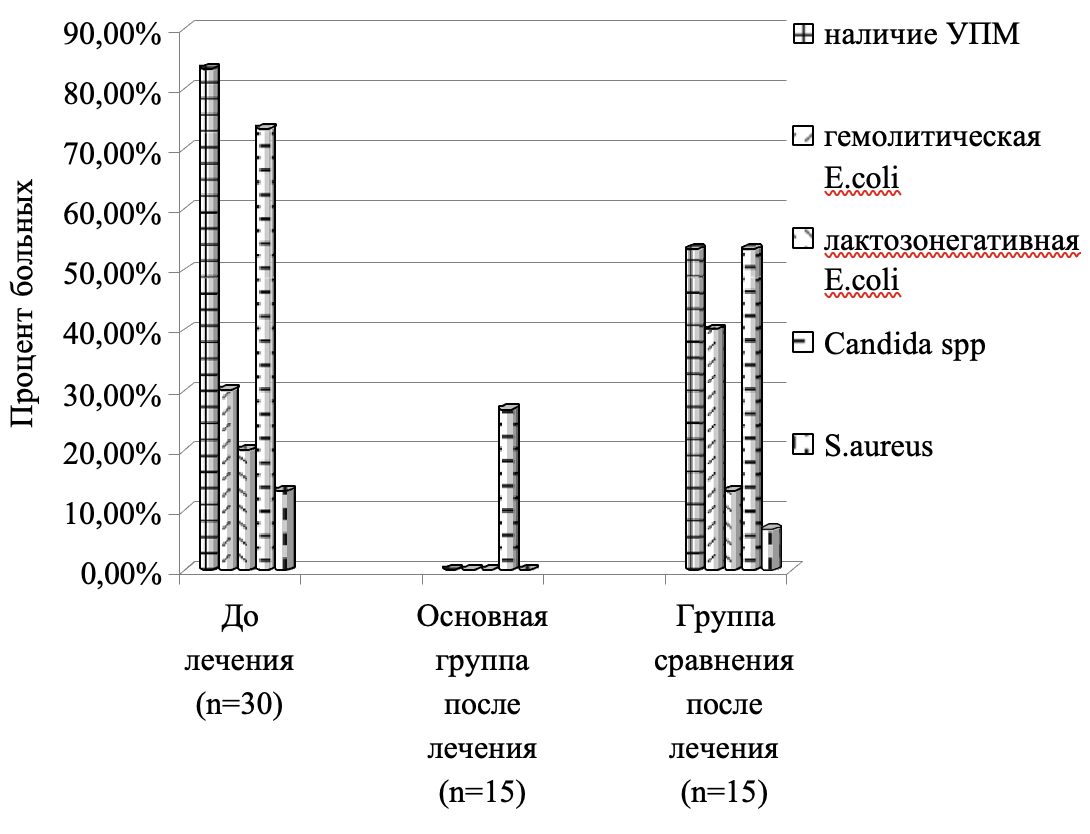
Рис. 3. Динамика клинически значимых микроорганизмов в ценозе кишечника
Проведена микробиологическая оценка эффективности метода лечения аллергических дерматозов с использованием ступенчатой энтеросорбции. Микробиологическая результативность проведенной терапии заключалась в нормализации количества бифидо- и лактобактерий, отсутствием условно-патогенных энтеробактерий, снижением в 2,7 раза количества грибов рода Candida, улучшении качественного состава биоты кишечника с исчезновением S.aureus, лактозонегативных и гемолитических E.coli.
ВЫВОДЫ
Исходя из изложенного, эфферентная терапия лиц с аллергическими заболеваниями патогенетически обоснована и занимает достойное место в арсенале современных средств реабилитации таких пациентов. Разработанный метод лечения аллергических дерматозов с использованием ступенчатой энтеросорбции терапии обладает высокой терапевтической эффективностью, хорошо переносится больными, являясь практически безопасным, позволяет даже без дополнительного назначения лакто- и бифидобактерий нормализовать биоценоз кишечника: уменьшить содержание патогенной микрофлоры и увеличить содержание полезной.
ЛИТЕРАТУРА
- Бержец В.М. Потенцированная форма аллергена для специфической аллерговакцинации больных с атопическими заболеваниями / А.И. Бержец, И.А. Коре- нева, М.Н. Мельникова // Вестник новых медицинскихтехнологий . –2005. – № 3/4 – С.67- 69
- Бондаренко В. М. Дисбактериозы кишечника у взрослых / В.М. Бондаренко, Н.М. Грачева, Т.В.Мацулевич. – М.: КМК. – 2003. – 224 с.
- Боткина А.С. Дерматологические проявления заболеваний ЖКТ / А.С. Боткина, С.В. Бельмер // Материалы XIV Конгресса детских гастроэнтерологов России. – М.,
- Буторова Л. И. Возможности коррекции нарушения кишечного микробиоценоза лактулозой / Л. И.Буторова, А. В. Калинин // Рос. журн. гастроэнтерол., гепатол., колопроктол. – 2008. – № 1. – С. 79-83
- Веселова Л.В. Состав микробиоценозов у больных аллергодерматозами / Л.В. Веселова, И.В. Хамаганова, М.И.Савина // IV научно-практическая конференция «Социально значимые заболевания в дерма- товенерологии. Диагностика, терапия, профилактика» – 2006. – С.36- 37.
- Гриневич В.Б. Принципы коррекции дисбиозов кишечника / В.Б. Гриневич, С.М. Захаренко, Г.А. Осипов // Лечащий врач. – 2008. – №6. – С.6-9.
- Копанев Ю.А. Дисбактериоз кишечника: микробиологические, иммунологические, клинические, микрологические аспекты. / Ю.А. Копанев, А.Л. Соколов // М., 2002. – 147с.
- Куваева И.Б. Микроэкологические и иммунные нарушения у детей / И.Б.Куваева, К.С.Ладодо. − М.: Медицина, 1991.
- Литинська Т.О. Роль і місце ферметів підшлункової залози в лікуванні хворих на гострі та хронічні захворювання шкіри / Т.О.Літинська // Укр. журн. дерматол., венерол., косметол. – 2009. – 4(35).
- Николаев В. Г. Энтеросорбция: состояние вопроса и перспективы на будущее / В.Г. Николаев // Вестник проблем биологии и медицины. – 2007. – № 4. – С.7-17.
- Новокшонов А. А. Клиническая эффективность нового энтеросорбента в комплексной терапии острых кишечных инфекций вирусной этиологии у детей / А.А. Новокшонов, Н.В. Соколова, Т.В. Бережкова,А.А.Сахарова // Лечащий Врач. – 2009. – № 7– C.78-80.
- Пухлик Б.М. Стан імунітету населення України та шляхи його корекції / Б.М. Пухлик // Ліки України.– – №9. – С.32- 33.
- Учайкин В.Ф. Энтеросорбция – роль энтеросорбентов в комплексной терапии острой и хронической гастроэнтерологической патологии. / В.Ф.Учайкин, А.А. Новок- шонов, Н.В.Соколова,Т.В.Бережкова // Пособие для врачей. – М., 2008.–24с.
- Методические указания по бактериологической диагностике дисбактериоза кишечника (для работников бак.лабораторий СЭС Приднепровской железной дороги). – Днепропетровск, 2001. – 7 с.
REFERENCES
- Berzhets V.M., Koreneva, I.A., Melnik- ova M.N. Potentsirovannaya forma allergena dlya spetsificheskoy allergovaktsinatsii bolnyih s atopicheskimi zabolevaniyami // Vestnik novyih meditsinskih tehnologiy .− 2005. − N 3/4. − S.67-69. (Russian)
- Bondarenko V.M., Gracheva N.M., Matsulevich T.V. Disbakteriozyi kishechnika u vzroslyih, – : KMK,2003. – 224 s. (Russian)
- Botkina A.S., Belmer S.V. Dermatologicheskie proyavleniya zabolevaniy ZhKT // Materialyi XIV Kongressa detskih gastroenterologov Rossii. − M., 2007. (Russian)
- Butorova I., Kalinin A.V. Vozmozhnosti korrektsii narusheniya kishechnogo mikrobiotsenoza laktulozoy // Ros. zhurn. gastroenterol., gepatol., koloproktol. – 2008. – N 1. – S. 79-83. (Russian)
- Veselova V., Hamaganova V., Savina M.I. Sostav mikrobiotsenozov u bolnyih allergodermatozami // IV nauchno-prakticheskaya konferentsiya «Sotsialno znachimyie zabolevaniya v dermatovenerologii. Diagnostika, terapiya, profilaktika».− 2006.− S.36-37.(Russian)
- Grinevich B., Zaharenko S.M., Osipov G.A. Printsipyi korrektsii disbiozov kishechnika // Lechaschiy vrach. – 2008. –N 6. – S.6-9. (Russian)
- Kopanev A., Sokolov A.L. Disbakterioz kishechnika: mikrobiologicheskie, immunologicheskie, klinicheskie, mikrologicheskie aspektyi. − M.,2002.– 147s. (Russian)
- Kuvaeva B., Ladodo K.S. Mikroekologicheskie i immunnyie narusheniya u detey. – M.: Meditsina, 1991. (Russian)
- Litinska O. Rol i mistse fermentIv pidshlunkovoyi zalozi v lIkuvannI hvorih na gostri ta hronIchnI zahvoryuvannya shkIri // Ukr. zhurn. dermatol., venerol., kosmetol. – 2009. – 4(35).(Ukrainian)
- Nikolaev V. G. Enterosorbtsiya: sostoyanie voprosa i perspektivyi na buduschee // Vestnik problem biologiii −2007. −N 4.− S.7-17. (Russian)
- Novokshonov A.A., Sokolova N.V., Berezhkova V., Saharova A.A. Klinicheskaya effektivnost novogo enterosorbenta v kompleksnoy terapii ostryih kishechnyih infektsiy virusnoy etiologii u detey // Lechaschiy Vrach. − 2009.−N 7.– C.78-80. (Russian)
- Puhlik B.M. Stan imunitetu naselennya Ukrayini ta shlyahi yogo korektsIyi // Liki Ukrayini. − 2010. − N9. − S.32-33.
- Uchaykin V.F., Novokshonov A.A., Sokolova N.V., Berezhkova T.V. Enterosorbtsiya – rol enterosorbentov v kompleksnoy terapii ostroy i hronicheskoy gastroenterologicheskoy patologii // Posobie dlya −M., 2008.–24s. (Russian)
- Metodicheskie ukazaniya po bakterioogicheskoy diagnostike disbakterioza kishechnika (dlya rabotnikov bak.laboratoriy SES Pridneprovskoy zheleznoy dorogi). – Dnepropetrovsk, 2001. – 7 s. (Russian)
СТУПІНЧАСТА ЕНТЕРОСОРБЦІЯ ЯК ОПТИМАЛЬНИЙ МЕТОД КОРЕКЦІЇ МІКРОБІОЦЕНОЗУ КИШЕЧНИКА У ХВОРИХ НА АЛЕРГОДЕРМАТОЗИ
Кутасевич Я.Ф., Олійник І.О., Джораева С.К., Мангушева В.Ю.
ДУ „Інститут дерматології та венерології НАМН України”
Резюме. У статті наводяться дані про терапевтичну ефективність ступінчастої ентеросорбції із застосуванням атоксілу і еліміналь-гелю у хворих на алергодерматози, враховуючи дослідження загального стану, суб’єктивних і об’єктивних скарг і мікробіоценозу кишечника до і після проведеної терапії.
Ключові слова: алергодерматози, мікрофлора кишечника, дисбактеріоз, ступінчаста ентеросорбція.
SPEED ENTEROSORBTION AS THE OPTIMAL METHOD OF CORRECTION OF GUT MICROBIOTA IN PATIENTS WITH ALLERGIC
Kutasevych Y.F., Oliinyk I.O., Joraevа S.K., Mangusheva V.Y.
SE «Institute of Dermatology and Venereology of National Medical Sciences of Ukraine»
Abstract.. The article presents data on the therapeutic efficacy of using speed enterosorption Atoxil andeliminal gel in patients with allergic dermatoses, given the general state of research, objective and subjective complaints and bowel microbiocenosis before and after the therapy.
Key words:: allergic dermatoses, the intestinal flora, dysbiosis, speed enterosorption.
Об авторах:
Кутасевич Янина Францевна – доктор мед. наук, профессор, директор ГУ «Институт дерматологии и венерологии НАМН Украины».
Олейник Ирина Александровна – доктор мед. наук, старший научный сотрудник, главный научный сотрудник отдела дерматологии, инфекционных и паразитарных заболеваний кожи ГУ «Институт дерматологии и венерологии НАМН Украины».
Джораева Светлана Карьягдыевна – кандидат мед. наук, заведующая лаборатории микробиологии ГУ «Институт дерматологии и венерологии НАМН Украины».
Мангушева Виктория Юрьевна – аспирант ГУ «Институт дерматологии и венерологии НАМН Украины».