УДК: 616.36 – 002.14-022:578.891-085.03
ПРИМЕНЕНИЕ ЭНТЕРОСОРБЕНТА “АТОКСИЛ” В ЛЕЧЕНИИ БОЛЬНЫХ ОСТРЫМИ ГЕПАТИТАМИ А И В
О.А. ГОЛУБОВСКАЯ, Н. Ч. КОРЧИНСКИЙ
Национальный медицинский университет имени А.А. Богомольца, кафедра инфекционных болезней
Ключові слова:
гепатиты А, В, лечение, энтеросорбенты, энтеросорбция, Атоксил
Актуальность совершенствования лечения больных гепатитами А и В обусловлена сохранением достаточно широкого распространения этих инфекций как в мире, таки в Украине, отсутствием этиотропного лечения при гепатите А (ГА) и согласованных рекомендаций по применению противовирусных препаратов при остром ГВ. Несмотря на снижение заболеваемости, существует большой экономический ущерб от гепатита А, который в 2006 г. составил в Российской Федерации более 1 млрд. руб., а в 2009 году – около 834 миллионов [10, 15]. Ранее ГА наблюдался преимущественно у детей и относился к группе так называемых “детских” заболеваний. У детей наблюдаются преимущественно легкие формы заболевания, без желтухи у 75-80% всех случаев болезни. Но в последнее время в Украине наблюдается значительный рост заболеваемости ГА среди взрослого населения с преобладанием более тяжелых форм, сопровождающихся желтухой, значительной продолжительностью заболевания и вообще более тяжелым течением. Заболеваемость ГА в Украине последние годы составила 24,8 – 26,3 случая на 100 000 населения, что существенно выше, чем в большинстве стран Европы [9,10].
Еще большее значение имеет проблема диагностики и лечения ГВ. Так, около трети населения земного шара имеет серологические признаки перенесенной или текущей инфекции, вызванной HBV. По оценкам экспертов ВОЗ этим возбудителем инфицированы от 300 до 400 миллионов человек. По различным сведениям, от 15 до 40% из них имеют прогрессирующий до цирроза печени (ЦП) и гепатоцеллюлярной карциномы (ГЦК) хронический гепатит В (ХГВ), который на любом этапе может осложниться печеночной недостаточностью и привести к летальным последствиям [7, 16, 19, 21]. Несмотря на доступность, эффективность и безопасность специфических вакцин, ГВ сохраняет 1-е место в мире среди всех причин смерти больных с патологией печени. От заболеваний печени, вызванных HBV, в мире ежегодно умирает от 1 до 2 млн. больных, в том числе только от ГЦК – от 0,5 до 1 млн. больных (5 место среди летальности от злокачественных опухолей). Ежегодно терминальные стадии HBV – инфекции являются причинами 5 – 10% всех трансплантаций печени в мире. Среди всех причин смерти последствия ХГВ занимают 10 место в мире [16, 18, 19, 21]. Специальные длительные исследования свидетельствуют, что через 5 лет после постановки диагноза ХГВ общая частота развития ЦП колеблется от 8 до 20%, а 5-летняя кумулятивная частота развития декомпенсации функций печени – около 20% при всего 5-летней вероятности выживания 80 – 83% больных с компенсированным ЦП. Ежегодная частота возникновения ГЦК у больных с ХГВ и ЦП составляет 2-5% [18, 20, 21].
В Украине носителями HBV являются не менее 1 млн человек. Каждый год только официально в нашей стране регистрируют 188 тысяч больных ХГ и ЦП, из них ежегодно погибает 6 тысяч. Маркеры HBV-инфекции: HBsAg и anti HBcor в Украине находят у доноров крови соответственно у 1,4% и 13,9%, у медицинских работников – у 5,4% и 26,8%, у лиц, употребляющих внутривенно наркотики – у 15,05% и 50,55% [7, 9].
Больные легкими и средней тяжести формами острых гепатитов А и В не нуждаются не только в этиотропной, но и в медикаментозной терапии вообще [17, 18]. Тем не менее, продолжается поиск препаратов, которые могут положительно повлиять на течение болезни, уменьшить длительность и выраженность интоксикационного, желтушного синдромов, при этом не оказывая серьезных побочных эффектов и не ухудшая исходы болезни [7, 8, 11].
К подобным препаратам, в первую очередь, относятся энтеросорбенты.
Энтеросорбция как один из методов детоксикационной терапии получила достаточно широкое распространение в клинической практике. Этот метод характеризуется простотой, безопасностью и экономичностью, поэтому успешно применяется при лечении различных заболеваний печени, в том числе и при ВГ [7, 8, 11, 12, 13].
Важными механизмами действия энтеросорбентов являются:
- связывание токсических веществ, попадающих в желудочно-кишечный тракт извне;
- связывание токсинов, диффундирующих в просвет кишечника из крови;
- связывание токсических веществ, выделяющихся с пищеварительными соками;
- поглощение токсических метаболитов, образующихся в желудочно-кишечном тракте;
- сорбционное изменение диеты за счет избирательного поглощения некоторых аминокислот и свободных желчных кислот;
- фиксация и перенос физиологически активных веществ (ферментов, желчных кислот и т.д.);
- изменение объема части пищи, которая не переваривается;
- каталитическое действие;
- обволакивающее и цитопротекторное действие;
- структуризация кишечного содержимого;
- образование агрегатов и флокулятов, содержащих микробы и вирусы;
- прямое бактерицидное действие;
- комплексообразование и хелатирование;
- модификация химического состава кишечного содержимого, которое становится неблагоприятным для размножения патогенной микрофлоры [8, 12,14].
В результате реализации указанных механизмов, энтеросорбенты уменьшают токсическую нагрузку на печень и почки. Энтеросорбенты, не всасываясь в кровь, тем не менее оказывают значительное системное воздействие на организм, устраняя нарушения липидного обмена, подавляя системную воспалительную реакцию, способствуя компенсации отдельных звеньев иммунной системы и улучшая функцию внутренних органов, что весьма важно у больных острыми вирусными гепатитами [8, 11, 12, 14].
Вследствие нарушения обменных процессов у больных с острыми ВГ развивается синдром метаболической интоксикации, обусловленный накоплением в крови молекул средней массы, которые оказывают токсическое воздействие на клетки печени, почек, на нейроны головного мозга. При тяжелом течении ВГ в кишечнике, а затем и в крови накапливаются аммиак и ароматические соединения, вызывающие развитие токсической энцефалопатии и печеночной комы [7, 12].
В Украине на сегодняшний день имеется достаточно большой выбор энтеросорбентов, которые имеют различные химическую структуру, физико-химические и органолептические свойства, отличаются различными клиническими эффектами. Площадь активной поверхности выступает основой для определения эффективности того или иного сорбента. Она обратно пропорциональна размеру частиц – чем меньше размеры частиц, тем больше суммарная площадь их активной поверхности. Поэтому от ее емкости зависит дозирование того или иного энтеросорбента, которое обеспечивает оптимальный терапевтический эффект [8, 12].
Таблица 1
Сравнение энтеросорбентов, обычно применяющихся в практическом здравоохранении Украины (В.Н. Нагорная, 2005)
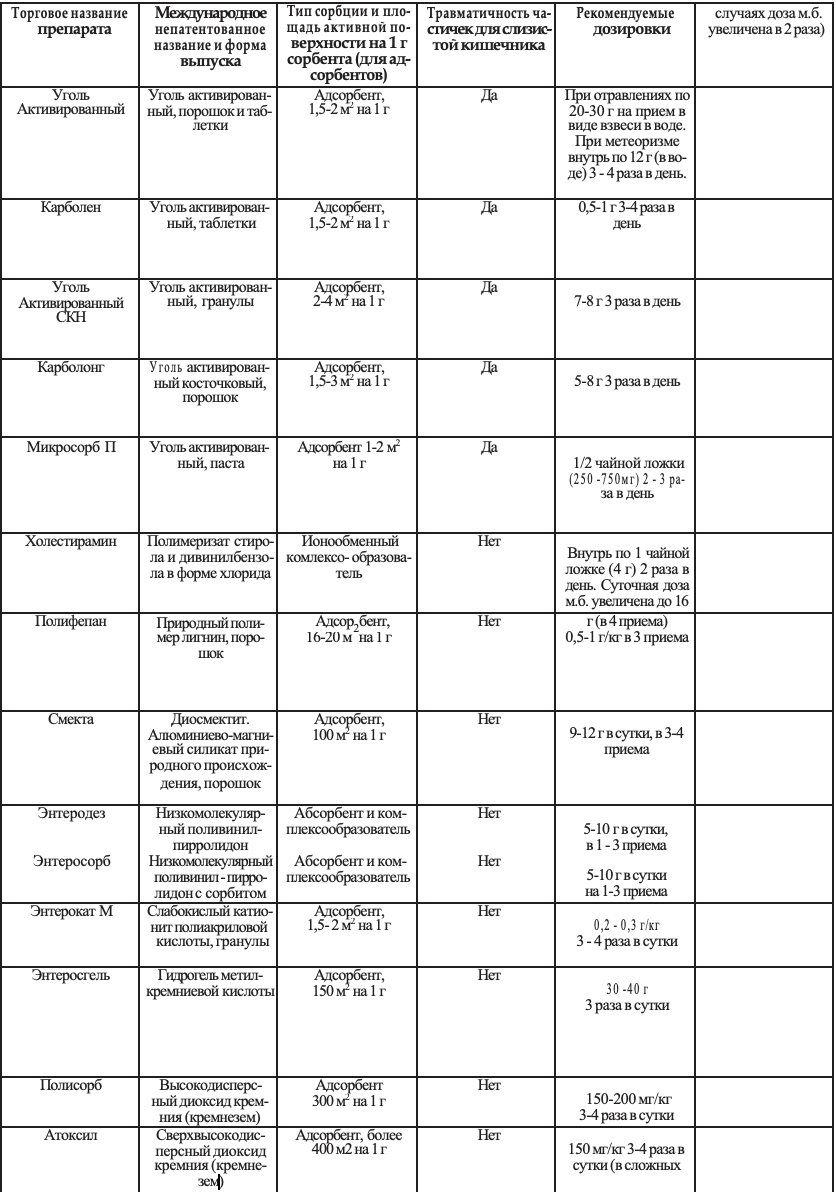
Сорбенты на основе активированного угля обладают малой площадью активной поверхности абсорбции на 1 грамм действующего вещества. Поэтому при значительной эндогенной интоксикации их необходимо принимать 20-30 грамм в сутки (80-120 таблеток активированного угля), что обуславливает гораздо меньшую привлекательность угольных сорбентов по сравнению с современными сорбентами, особенно созданными на основе диоксидов кремния [8].
Сравнение энтеросорбентов, обычно применяющихся в практическом здравоохранении Украины, приведено в Таблице 1. Благодаря высокой сорбционной активности препаратов диоксида кремния (Таблица 1) более интенсивно происходит абсорбция и выведение из ЖКТ эндогенных и экзогенных токсических веществ, в частности, продуктов жизнедеятельности патогенных микроорганизмов. Препараты не всасываются из пищеварительного канала, при этом оказывая мощную системную дезинтоксикацию.
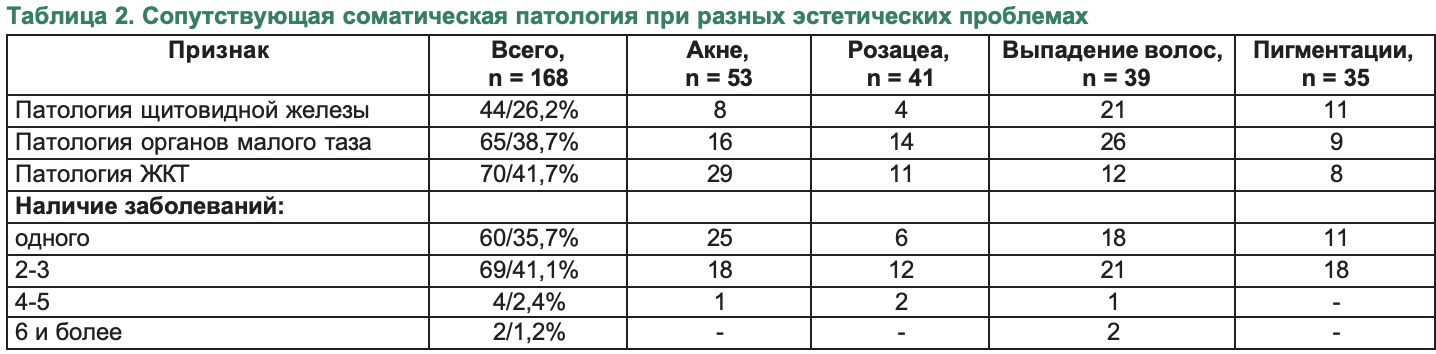
Следует отметить также избирательность адсорбции препаратов на основе диоксида кремния, что определяет их преимущества по сравнению с другими препаратами [8, 12, 13]. Соответствующие материалы представлены в Таблице 2. Благодаря перечисленным выше свойствам, препараты на основе диоксида кремния оказывали положительный эффект при:
- диарреях инфекционного и неинфекционного генеза;
- колитах;
- острых и хронических вирусных гепатитах;
- ботулизме;
- кишечном токсикозе;
- хронических обструктивных заболеваниях легких;
- бронхиальной астме;
- хронической почечной недостаточности;
- экземе, псориазе;
- атопическом дерматите;
- поздних гестозах беременных;
- в хирургической практике;
- в токсикологии;
- в онкологии [1, 3,4,5,6,7, 8,11,12,13,14].
Проведенные ранее клинические исследования [7,8,11] касаются преимущественно гидрогеля метилкремниевой кислоты, тогда как работ по изучению эффективности других препаратов на основе диоксида кремния немного. В то же время самыми действенными в борьбе с интоксикацией у больных с различной патологией печени считаются сорбенты, приготовленные именно на основе диоксида кремния, в частности Атоксил, который лишь начинает внедряться в гепатологическую и инфекционную практику [4,5,7,11,12].
Препарат “АТОКСИЛ” (кремния диоксид), который производит ООО “Орисил фарм”, это диоксид кремния, представляет собой легкий аморфный порошок белого цвета, без вкуса и запаха, в бутылках ёмкостью 250 мл. 1 бутылка содержит 10,0 гр. высокодисперсного порошка кремния диоксида. Площадь его активной сорбции равняется более 400 м² на 1 г сухого вещества, что является одним из наибольших показателей среди подобных препаратов (Таблица 1). АТОКСИЛ является энтеросорбентом с выраженными сорбционными свойствами, проявляет детоксикационное, а при местном применении – и противомикробное и ранозаживляющее действие [3,5,11,14]. Препарат адсорбирует из пищеварительного тракта и выводит из организма эндогенные и экзогенные токсические вещества различного происхождения, обладает высокой адсорбционной активностью в отношении микроорганизмов и белков, в том числе и микробных токсинов. При этом ухудшается десорбция связанных белков и токсинов как через рану, так и через стенки кишечника. АТОКСИЛ способствует транспорту из внутренней среды организма (кровь, лимфа) в пищеварительный тракт за счёт концентрационных и соматических градиентов разнообразных токсических продуктов, в том числе средних молекул, олигопептидов, аминов и других веществ с последующим выведением из организма. При этом он практически не всасывается из кишечника и раны [3,8,13,14]. Атоксил противопоказан пациентам с обострением язвенной болезни 12-перстной кишки и желудка, эрозиями и язвами слизистой оболочки толстого и тонкого отделов кишечника, с кишечной непроходимостью, с повышенной чувствительностью к диоксиду кремния. Атоксил не назначают детям в возрасте до одного года и беременным [5,14].
Как показали клинико-лабораторные исследования, препарат АТОКСИЛ является эффективным в комплексном лечении ожогов и профилактике инфекционных осложнений у обожжённых. Он удовлетворительно переносился больными при пероральном и местном применении, не вызывая при этом побочных эффектов. Комплексная дезинтоксикационная терапия с использованием препарата АТОКСИЛ приводила к снижению токсических свойств сыворотки крови, обеспечивала существенное снижение токсического воздействия на нейтрофильные гранулоциты периферической крови, на что указывали интегральные индексы интоксикации [14]. Получено экспериментальное подтверждение положительного влияния Атоксила на периапикальные ткани при лечении периодонтитов [3]. Комбинации Атоксила и кверцетина улучшала результаты лечения больных пептической язвой двенадцатиперстной кишки на фоне гипертонической болезни, устраняя при этом нарушения метаболических показателей [1,2]. Атоксил повышал эффективность комплексной терапии аскаридоза у детей [4]. Подтверждена эффективность и безопасность лечения Атоксилом острых кишечных инфекций у детей [5]. В то же время мы не нашли сведений о применении этого препарата у больных острыми или хроническими вирусными гепатитами. Это и определило наш выбор в исследовании клинической эффективности этого энтеросорбента у больных острыми ВГ.
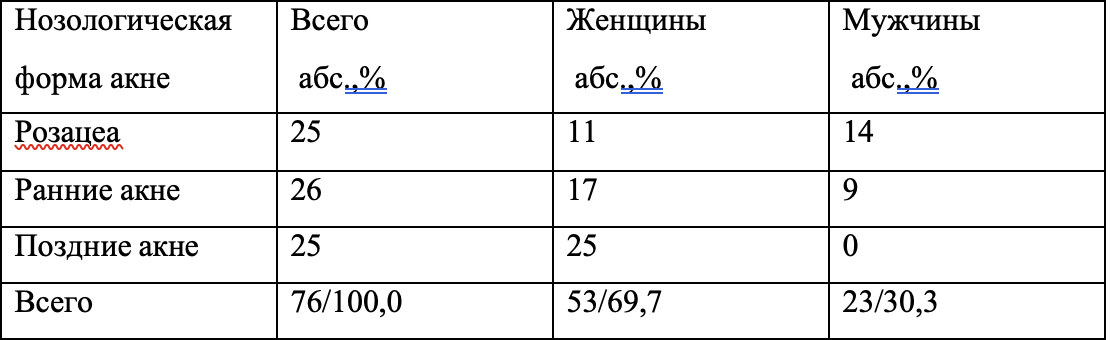
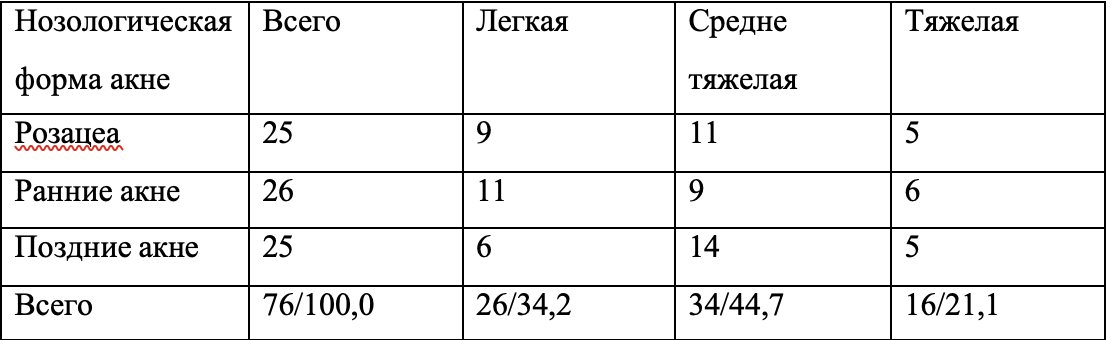
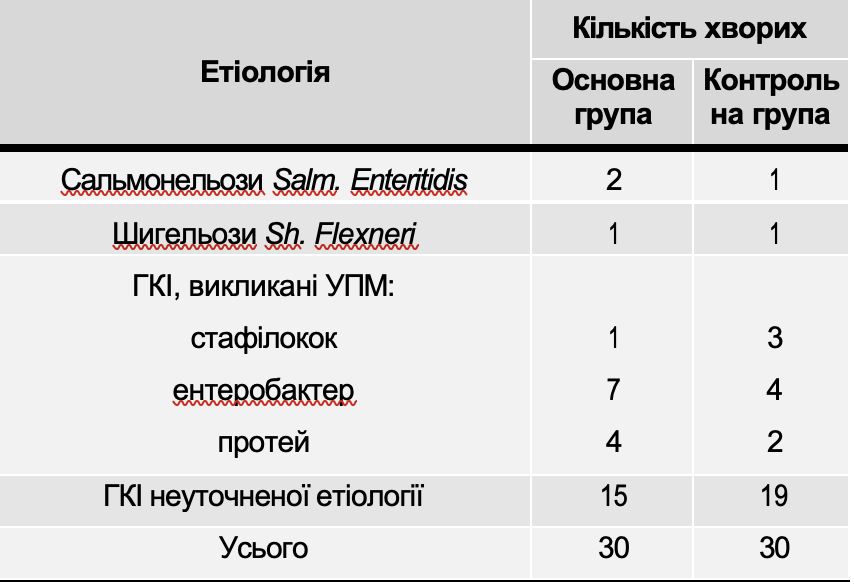
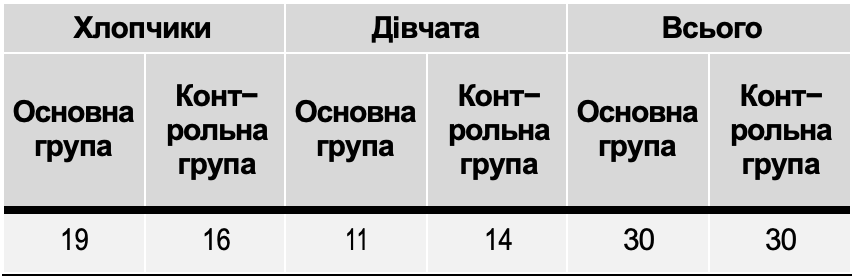
Согласно поставленным задачам, в клинике инфекционных болезней НМУ в течение 2010–2012 гг. обследовали и наблюдали 71 больного ГА и острым ГВ с не тяжелым течением болезни в возрасте от 18 до 62 лет (средний возраст пациентов – 34,6±8,2 года). Преобладали больные в возрасте от 18 до 35 лет (52 человека, 73%). Мужчин было 32, женщин – 39 человек. Легкая желтушная форма ВГ была у 19 (26,8%), средней тяжести – у 52 (73,2%) больных. Для изучения терапевтического действия энтеросорбента Атоксила всех больных методом рандомизации разделили на две сопоставимые по возрасту, полу, характеру сопутствующих заболеваний группы. Поскольку не изучали действие препарата на длительность HBs-антигенемии, вирусемии, сочли возможным объединить в одной группе больных с ГА и острым ГВ, распределение которых в группах также не отличалось: по 7 больных ГА в каждой группе (Рис. 1).
Больные 1-й группы (36 человек) получали лечение Атоксилом. Больные 2-й группы (35 человек) получали только базисную терапию. Общая характеристика групп больных представлена на Рис. 1.
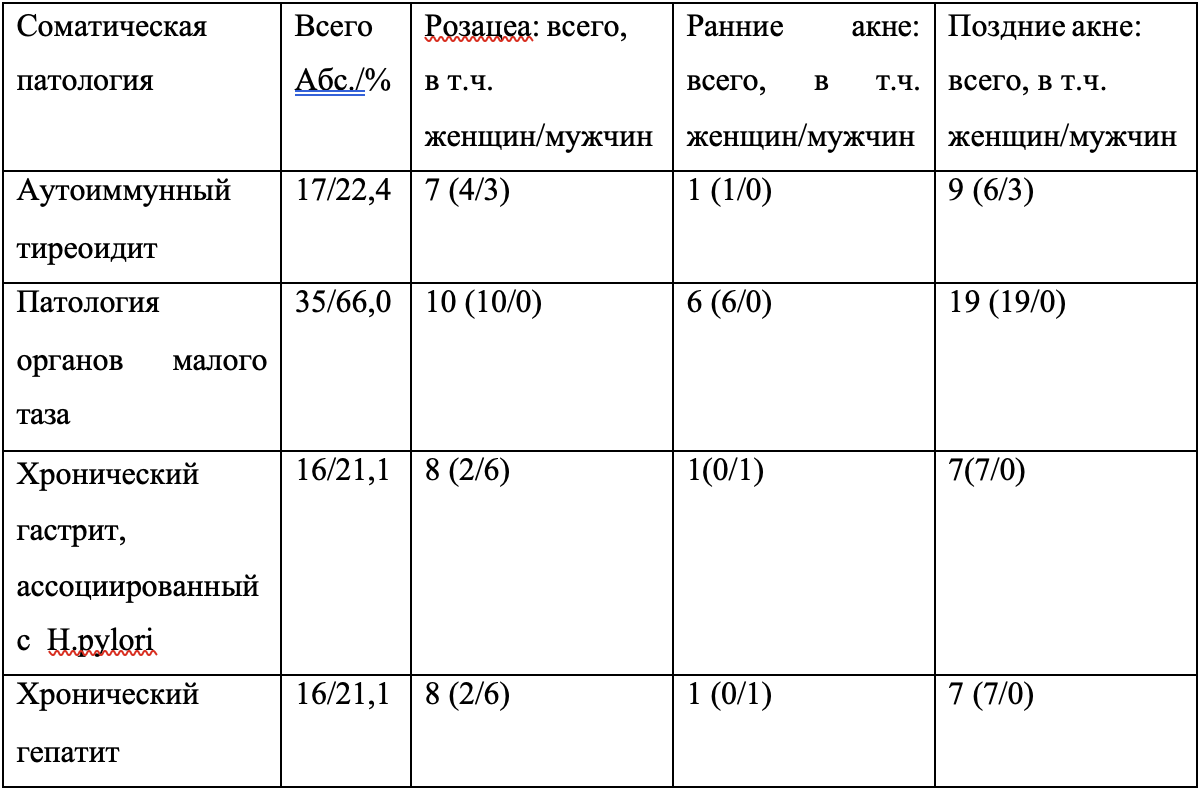
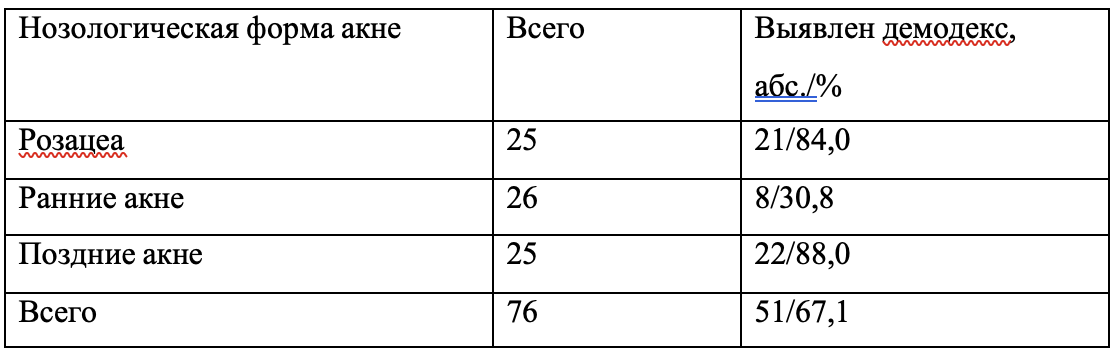
Как видно по данным, приведенным на Рис. 1, по основным параметрам – полу, возрасту, тяжести течения ВГ и его этиологии группы больных были сопоставимы. Наиболее частым сопутствующим заболеванием были хронический панкреатит у 43 (60,6%), обострение хронического гастродуоденита – у 21 (29,6%), холецистита – у 19 (26,8%), жировая болезнь печени в виде неалкогольного и алкогольного стеатогепатита – у 16 (22,5%), хронический бронхит – у 9 (14,6%). На Рис. 2 представлена характеристика групп больных в зависимости от характера сопутствующей патологии, которая чаще всего встречалась на фоне ВГ.
Как видно по материалам, приведенным на Рис. 2, значительных отличий по характеру сопутствующей патологии между 1-й и 2-й группами также не было.
Больные с тяжелой соматической сопутствующей патологией (декомпенсированный сахарный диабет, выраженный атеросклероз, тяжелая артериальная гипертония и т.д.) в исследование не включались, поскольку требовали постоянного приема значительного количества медикаментозных препаратов. У всех больных исключены ВИЧ и HCV – инфекция.
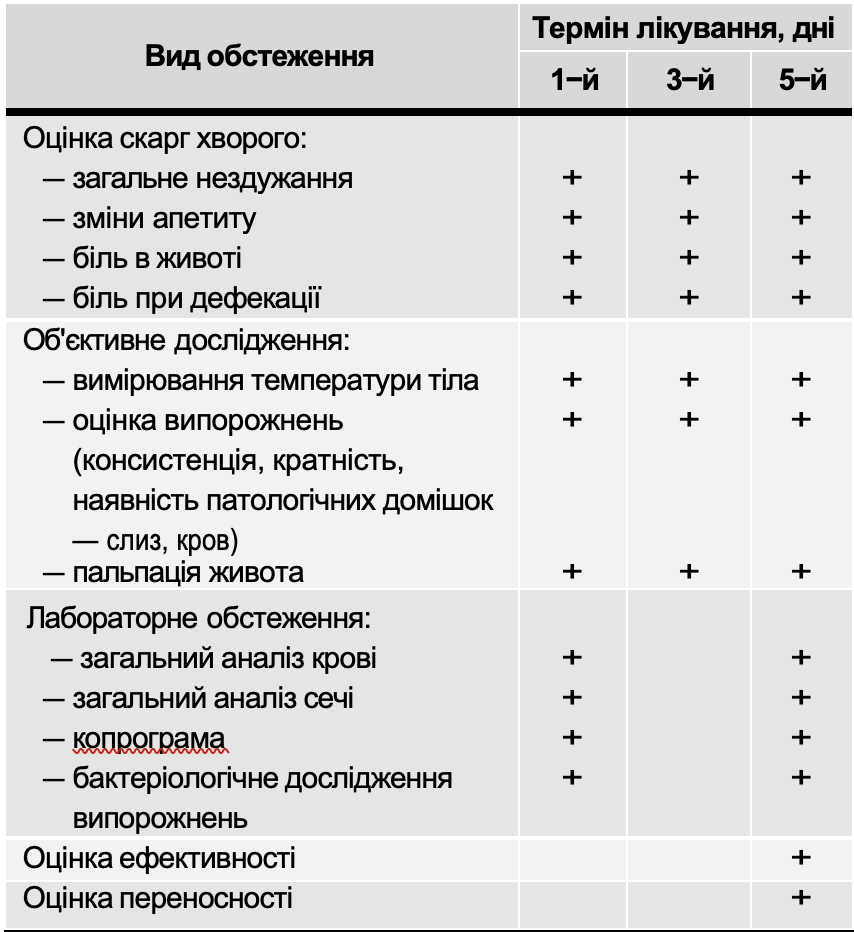
У всех больных в динамике исследовали показатели общего анализа крови, содержание в крови глюкозы, общего белка, общего билирубина и его фракций, мочевины, креатинина, активность АлАТ и АсАТ при помощи общепринятых методик с использованием стандартных реактивов и биохимического анализатора Humalaser. Проводилось ультразвуковое исследование печени, желчного пузыря, поджелудочной железы, селезенки, почек с использованием серой шкалы на аппарате эксперт–класса Voluson 730 SSD. При помощи иммуноферментного анализа (ИФА) диагноз ГА специфически подтвержден у 14 больных наличием в крови AntiHAV Ig М, острого ГВ – у 57 больных наличием в крови HBsAg и anti HBcor Ig M. В сомнительных случаях (дифференциация с хроническим ГВ) дополнительно количественно определяли anti HBcor IgG, HBeAg, anti HBe Ig G (ИФА).
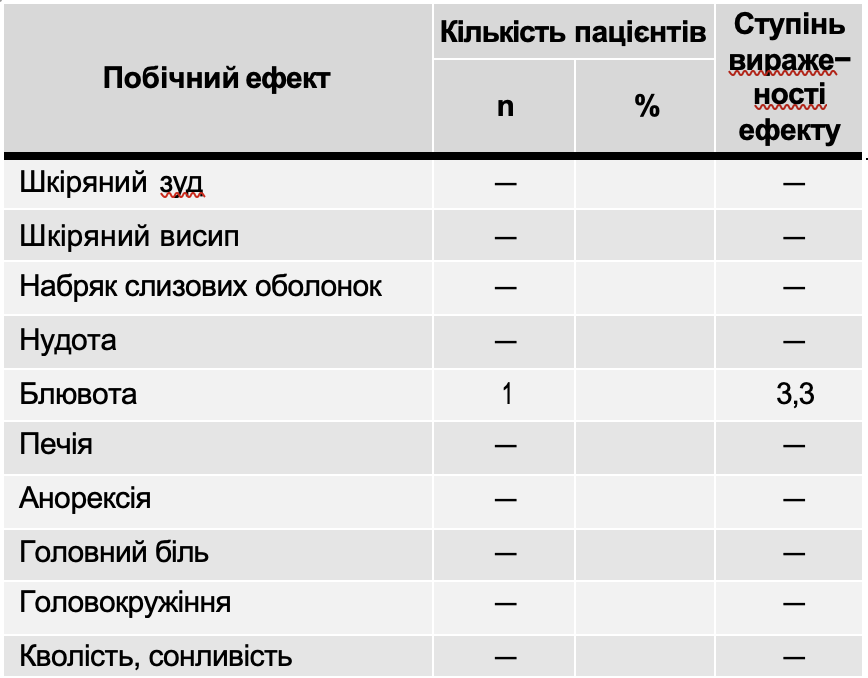
36 человек первой группы на фоне общепризнанной базисной терапии (постельный режим, стол № 5а, обильное питье) с момента госпитализации в клинику (в среднем, с 4,3±2,1 дня желтушного периода) получали Атоксил из расчета 0,2 г на кг массы тела в сутки (в среднем 12 г) внутрь в 3 приема за 2–1,5 часа до приема пищи в течение 2-х недель. 35 человек второй группы получали в этом же периоде болезни только базисную терапию. Ни у одного из больных не отмечено серьезных побочных действий Атоксила, которые требовали бы отмены препарата. У одного больного с сопутствующим обострением хронического гастродуоденита отмечено кратковременное усиление тошноты, у 3-х больных – усиление запоров, потребовавшее назначение препаратов Лактулозы.
Таблица 2
Селективность адсорбции препаратов на основе диоксида кремния (по А.А. Чуйко, 2003)
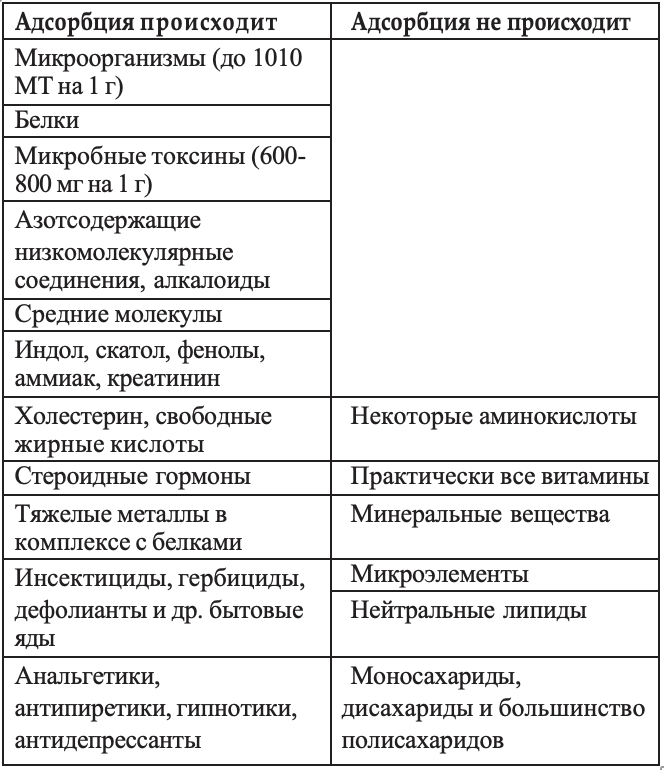
Рис 1. Общая характеристика групп больных
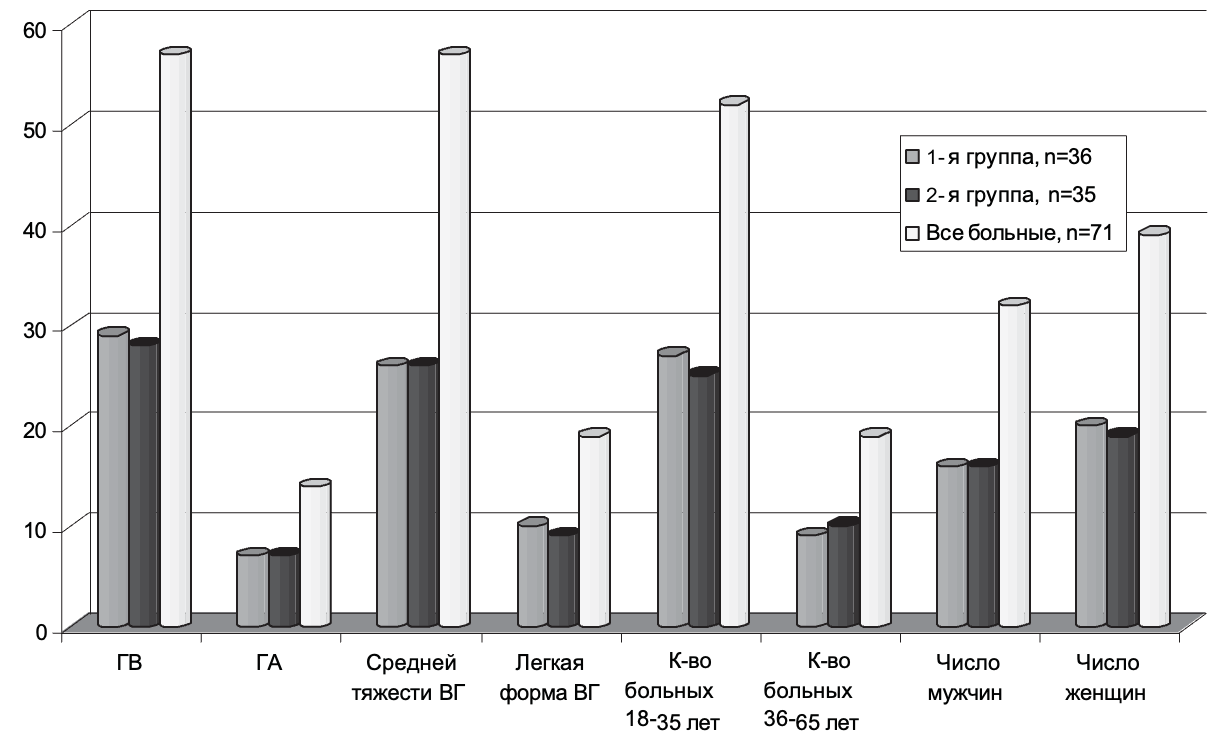
Таблица 3
Сравнение продолжительности клинических симтомов желтушного периода острых ВГ у больных, получавших Атоксил и лечившихся без него

Рис. 2. Характеристика групп больных в зависимости от сопутствующей патологии.
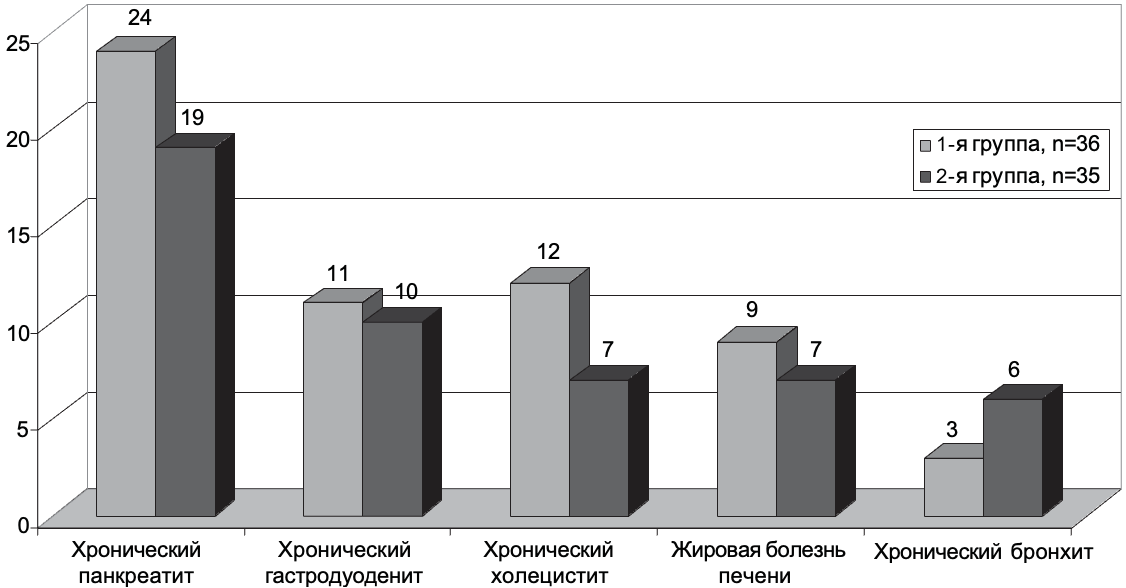
Таблица 4
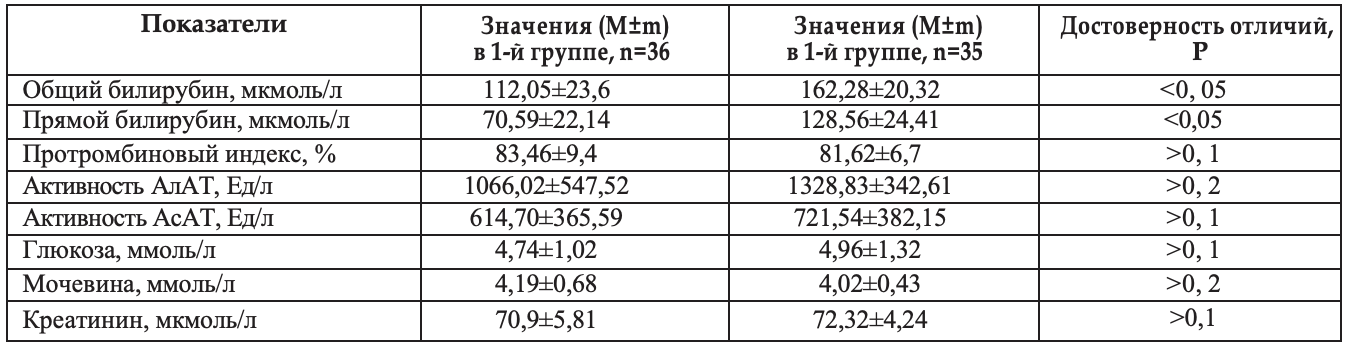
Сравнение средних величин основных биохимических показателей крови у больных обеих групп до лечения Атоксилом
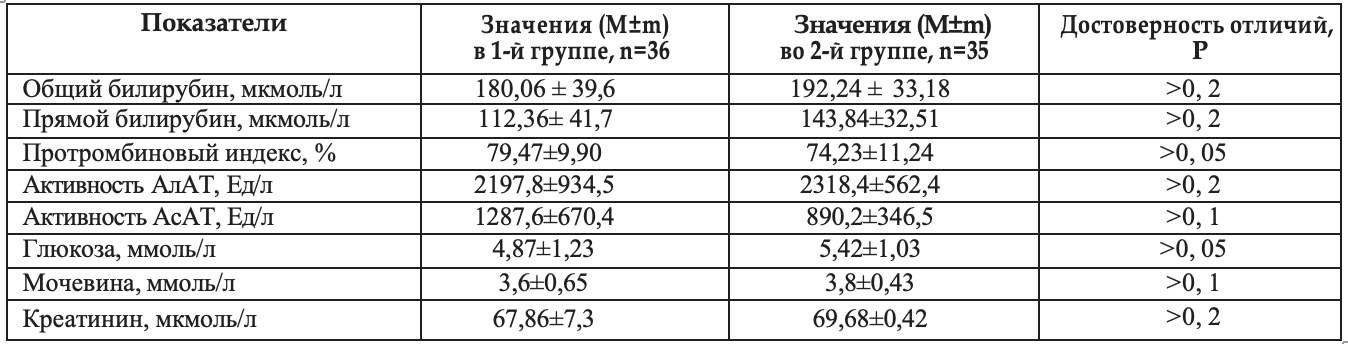
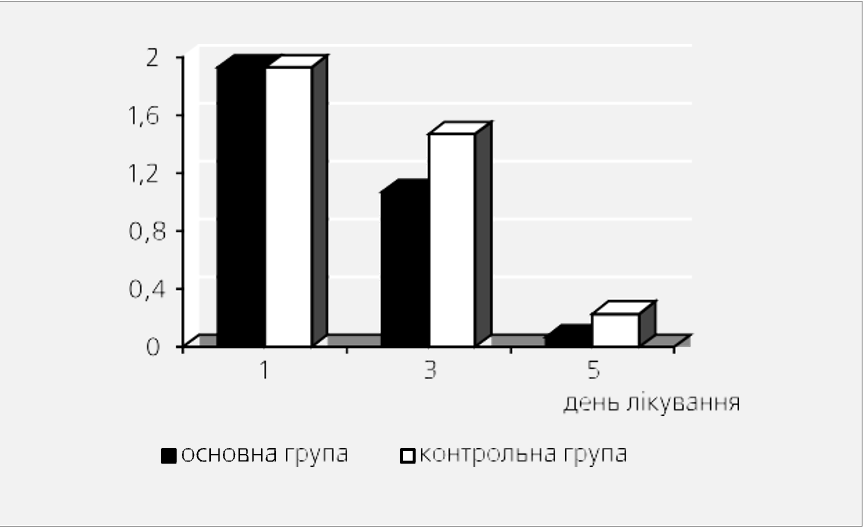
Рис. 3. Сопоставление средних показателей продолжительности клинических симтомов при лечении больных Атоксилом (n=36) и без него (n=35)
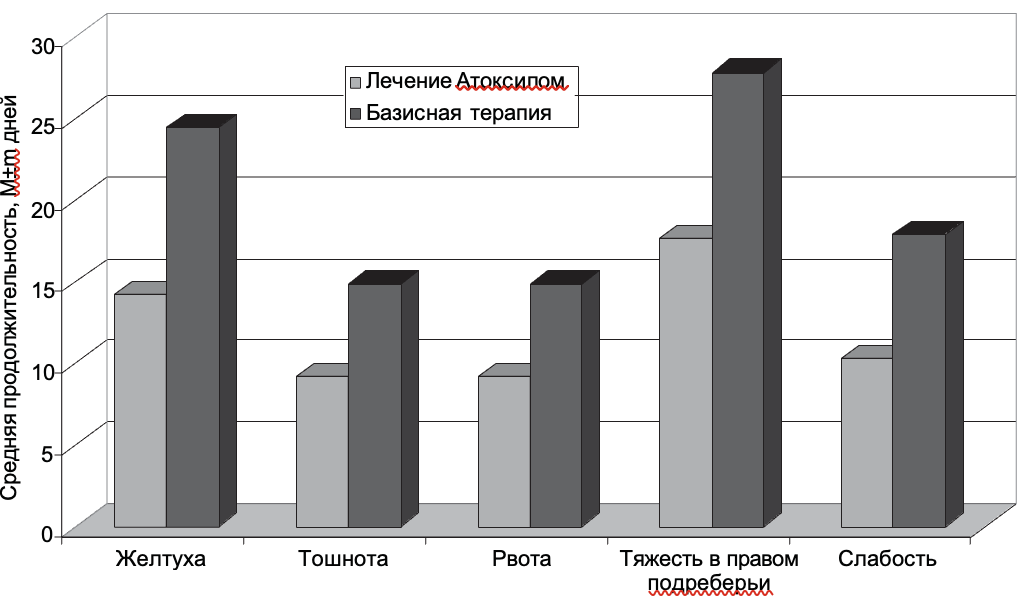
Таблица 5
Сравнение средних величин основных биохимических показателей крови у больных обеих групп после лечения Атоксилом
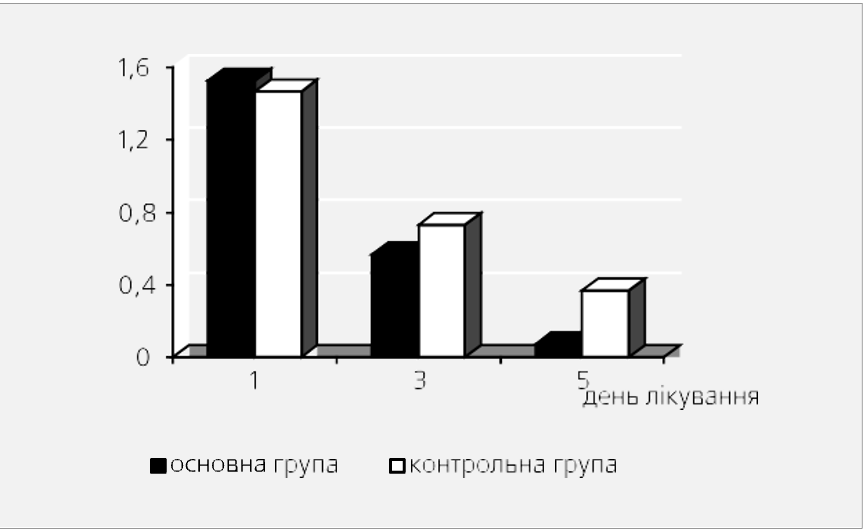
В обеих группах анализировали продолжительность симптомов болезни. Соответствующие данные представлены в Таблице 3. Как свидетельствуют данные, приведенные в таблице 3, лечение Атоксилом достоверно (Р<0,05) сокращало длительность желтухи, тяжести в правом подреберье, тошноты, рвоты, общей слабости, подтверждая тем самым свое выраженное дезинтоксикационное действие. Соответствующие данные приведены на Рис. 3.
Как свидетельствуют данные, приведенные на Рис. 3, лечение Атоксилом вызывает достоверно (Р<0,05) более быстрое обратное развитие таких симптомов болезни, как желтуха, слабость, тяжесть в правом подреберье, тошнота, рвота по сравнению со средней продолжительностью аналогичных симптомов у больных группы сравнения.
Основные анализируемые биохимические показатели крови до начала болезни в обеих группах достоверно не отличались (Таблица 4), поэтому анализ показателей проведен нами после 2-х недель лечения Атоксилом.
Как свидетельствуют материалы, приведенные в таблице 4, достоверных отличий не было ни по одному из сравниваемых средних показателей биохимических показателей крови. В таблице 5 представлены результаты сопоставления средних величин основных биохимических показателей крови после лечения Атоксилом.
Как свидетельствуют материалы, приведенные в таблице 5, после лечения Атоксилом достоверно больше снизились средние показатели общего билирубина крови и его прямой фракции по сравнению с таковыми у больных, не получавших энтеросорбенты (Р<0,05 и <0,05 соответственно). Достоверных отличий средних показателей активности АлАТ, АсАТ, ПТИ, содержания глюкозы, креатинина и мочевины крови у больных, леченных Атоксилом, по сравнению с таковыми у группы сравнения не получено.
Таким образом, лечение Атоксилом в дозе 12 г/сутки внутрь в течение 2-х недель больных с не тяжелыми острыми гепатитами А и В достоверно уменьшает длительность диспептического, интоксикационного синдромов, желтушного периода, снижает уровень общего и прямого билирубина по сравнению с такими же показателями у больных, которые в эти же сроки болезни получали только базисную терапию. Препарат хорошо переносится, не вызывает отрицательных эмоций при его приеме, сравнительно недорог, удобен в применении, не вызывает серьезных побочных явлений, что позволяет рекомендовать его для более широкого применения в лечении острых вирусных гепатитов.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
- Белокобыльская Д.В. Изменения содержания лейкотриенов и активности липопероксидации под влиянием комбинации атоксила и квер-етина в динамике лечения больных пептической язвой двенадцатиперстной кишки в сочетании с гипертонической болезнью / Д.В. Белокобыльская// Український медичний альманах. – Том 13, №4. – С. 30-32.
- Бурмак Ю.Г. Изменение некоторых метаболических показателей в динамике лечения больных пептической язвой двенадцатиперстной кишки в сочетании с гипертонической болезнью / Ю.Г. Бурмак , Д.В. Белокобыльская //Таврический медико-биологический вестник. – 2010. – том 13, № 1 (49). – С. 23 – 25.
- Дорофеева Н.Г. Экспериментальное под-верждение влияния сорбентов на периапикальные ткани при лечении периодонтитов [Текст] /Н.Г. Дорофеева, Т.А. Чалая , М. Ерохина, А.Обидин // Український медичний альманах. – 2008. – Том 11, №5. – С. 61-62.
- Корнева В.В. Оценка эффективности энтеросорбента Атоксила в комплексном лечении аскаридоза у детей / В.В. Корнева, Л.В. Курило, В.Г. Козачук,Е.А. Боярская, М.А. Капичина //Современная Педиатрия. – -№3(37). – С.66-68.
- Крамарєв С.О. Вивчення ефективності і безпечності ентеросорбенту Атоксіл при гострих кишкових інфекціях у дітей / С.О.Крамарєв, О.А.Дмітрієва // Сучасна педіатрія. – – № 3. – С. 93-97.
- Кузнецов С.В. Эффективность энтеросоребента Белый уголь в комплексной терапии гельминтозов у детей / С.В. Кузнецов // Здоровье ребенка.– – №4 . – с. 30-33.
- Лікування хворих на цироз печінки переважно вірусної етіології, ускладнений асцитом /Ж.І. Возіанова , О.А. Голубовська, М.Ч. Корчинський //Мистецтво лікування, 2005. – №5(21). – С. 22 – 27.
- Медицинская химия и клиническое применение диоксида кремния/ под ред. акад. НАН Украины А.А.Чуйко.- Киев: Наукова думка. – – 416 с.
- Міністерство охорони здоров’я України //НАКАЗ № 296 від 19.05.2011 р. “Про внесення змін до Наказу МОЗ України від 03.02.2006 № 48”
- Михайлов М.И., Шахгильдян И.В., Онищенко Г.Г. Энтеральные вирусные гепатиты (этиология, эпидемиология, диагностика, профилактика) – Москва: ВУНМЦ, 2007 г.- 352 с.
- Мороз Л.В., Палій І.Г. Застосування препарату Ентеросгель у комплексній терапії хворих на гострі вірусні гепатити із супутнім дисбактеріозом кишечника / Л.В. Мороз, І.Г. Палій // Медико-біологічні аспекти застосування ентеросорбенту “Ентеросгель” для лікування різних захворювань: Збірка вибраних наукових статей. –Київ: “Богдана”, 2010. -С.83-88.
- Нагорная Н.В.Использование энтеросорбции в лечении атопического дерматита / Н.В.Нагорная, Е.В.Бордюгова, А.В.Дубовая //Современная педиатрия. – 2005. – № 4(9). – С.67 – 70.
- Палий И.Г. Современный взгляд на проблему энтеросорбции: выбор оптимального препарата / И.Г. Палий, И.Г. Резниченко // Новости медицины и фармации. – №11 (217). – С. 15-17.
- Применение препарата “Атоксил” в комплексном лечении обожженных / Э.Я. Фисталь, И.И. Сперанский, В.В. Арефьев, Е.Г. Тимошенко, М.В. Лобачёва, Е.А. Писаренко // Комбустиология. – № 27.- С. 24 -28.
- Шахгильдян И.В. Оценка итогов вакцинопрофилактики гепатита А в отдельных регионах Российской федерации. Нужна ли сегодня плановая вакцинация детей против гепатита АṢ [Текст ]/ И.В. Шахгильдян, М.И. Михайлов, О.Н. Ершова, П.А. Хухлович, В.А. Хасанова, И.Н.Лыткина, Н.И. Шулакова, В.В. Романенко, А.И. Юровских, А.А. Ясинский //Гепатологія. – – № 1. – С.34-40.
- Carey D. The prevalence and natural history of hepatitis B in the 21st century / Cleve. Clin Med., 2009. – N 76 (Suppl.3). – P. 2 – 5.
- Dienstag J.L. Drug Therapy: Hepatitis B Virus //N. Engl. J. Med., 2008. – Vol 359, N. 14. – Р. 1486-1500.
- European Association for the Study of the Liver ( EASL), Clinical Practice Guidelines: Management of chronic hepatitis B. //J. Hepatol., 2009.– № 50(2). – Р. 227-242.
- Elgouhari M., Abu-Rajab Tamimi T.I., Carey W.D. Hepatitis B virus infection: understanding its epidemiology, course, and diagnosis/ Cleve.Clin.J.Med., 2008. – N 75 (12). – P. 881 – 889.
- Lok S., McMahon B.J. Chronic hepatitis B: update 2009 / Hepatology, 2009. – N 50 (3). – P. 661-662.
- Mitchell A. E., Colvin H. M., Beasley R. P. Institute of Medicine Recommendations for The Prevention and Control of Hepatitis B and C / Hepatology, – Vol.51 (N 3). – P. 729-733.
УДК: 616.36-002-022.7-07:578.27:578.891
ЗАСТОСУВАННЯ ЕНТЕРОСОРБЕНТУ “АТОКСИЛ” У ЛІКУВАННІ ХВОРИХ НА ГОСТРI ГЕПАТИТИ А ТА В
У статті проводиться аналіз власних досліджень ефективності терапії 37 хворих на гепатити А і В ентеросорбентом Атоксилом, якізнаходились на лікуванні в клініці інфекційних хвороб НМУ у 2011 – 2012 рр. Результати лікування порівнювали з відповідними показниками у 36 хворихгрупи порівнян- ня, яка мала такий самий склад за віком, статтю, тяжкістю перебігу, характером супутньої пато- логії. Отримані результати свідчать про доцільність проведення лікування Атоксилом хворих на ГА та гострий ГВ при не тяжкому перебігу хвороби, що дозволяє достовірно скоротити тривалість інтоксикаційного періоду, жовтяниці, зменшити рівень загального та прямого білірубіну крові порівняно з відповідним ипоказниками у хворих, що не отримували ентеросорбенти. Препарат добре переносив- ся хворими та не викликав серйозних побічних явищ.
О.А.Голубовська, М.Ч.Корчинський
UDC: 616.36-002-022.7-07:578.27:578.891
ENTEROSORBENT “ATOKSYL” USE IN THE TREATMENT OF PATIENTS WITH ACUTE HEPATITIS A AND B
In the article the analysis of their research the effectiveness of therapy 37 patients with hepatitis A and B enterosorbent Atoksyl who were treated at theclinic of infectious diseases NMU in 2011 – 2012. Results of treatment compared with the cor- responding parameters in 36 patients with com- parison group who had the same composition by age, sex, severity, nature of comorbidity. The results demonstrate the feasibility of a treatment Atoksyl patients with hepatitis A and acute hepatitis B with no serious disease, which allows significantly reduce the intoxication period, jaundice, reduced levels of total and direct bilirubin levels compared with the corresponding rates in patients not receiving enterosorbents. The drug was well tolerated by patients and did not cause serious side effects.
Golubovskaya, M. Korchynskyi